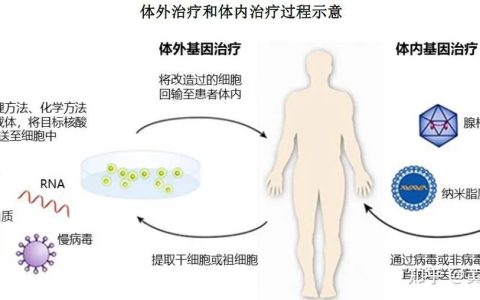
干细胞的制备需要在完全无菌的状态下进行,对环境和设施设备有极高的要求。国家规定细胞治疗产品需按照药品生产质量管理规范(GMP),在B+A级的洁净级别的实验室/生产车间进行生产,即与干细胞制备直接相关的操作应在B级背景下的A级环境中进行。因此,通过实验室/生产车间的洁净度等级可以判断一家细胞公司的科研平台是否达标:有没有达到B+A级?是否有权威的第三方检测认证机构出具的检测报告?
干细胞制剂看起来像是一袋普通液体,但制备、储存条件,技术等差异造成其质量、活力、活性、功效都会有很大差异。中国食品药品检定研究院(简称“中检院”)是国家检验⽣物制品药品质量的法定机构,也是三甲医院唯⼀认可的临床级细胞检验机构。获得中检院的细胞质量复核报告,证明其干细胞质量达到了临床级别。另外,为考察生物制品的均一性、稳定性以及验证工艺,送检样品批次数量应至少为三批。因此可以通过这样判断:是否获得中检院质量复核认定?送检批次数量是多少?获得多少份报告?
大部分的干细胞临床研究项目是由干细胞公司与医院合作展开,因此从医院合作也可以验证公司的实力,例如:是否与国内排名靠前的三级甲等医院在合作?合作的医院有多少家?
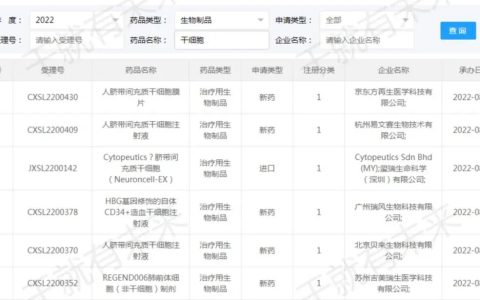
最后,还有一个最简单的判断方法,那就是让国家监管机构替我们判断干细胞公司的实力:有没有干细胞IND(临床试验申请)?是否已经获批临床试验?
干细胞是生命的保障,基于临床效果和生命安全的考量,还请擦亮眼睛选择靠谱的干细胞公司,才能保证干细胞的高标准、高质量。
编辑:小果果,转载请注明出处:https://www.cells88.com/zixun/hydt/34243.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫