斯坦福大学打开iPSC新的大门,可制造针对广谱恶性肿瘤的疫苗
而话说回来,针对iPSCs的临床治疗,究竟有怎样的前景?除了早前我们说的致瘤性和DNA损害的问题外,单就临床效果而言,我个人就一直是持一个保留的态度的。
本文抛开一部分希望通过细胞和组织替代作用的iPSCs临床应用不谈,譬如生成视网膜细胞RPE以治疗黄斑变性等。
单就另外一部分iPSCs的临床应用而言,我们当前主流的认识是外泌体在起作用,这同时也是间充质干细胞治疗的主要机制。
那么直接比较MSCs和iPSCs的外泌体表达和特征,不就可以知晓MSCs和iPSCs的临床治疗潜力大小了?
恰好,《Experimental Cell Research》发表了一篇新的文章,正好做了这方面工作,供大家参考。

文章的主要观点是:
- 我们的蛋白质组分析显示,间充质干细胞外泌体具有更强的蛋白质谱和更高的表达水平。
- 在脐带间充质干细胞外泌体中发现了更高的蛋白强度和更独特的蛋白。
- 生物信息学分析揭示了已鉴定的蛋白质对许多疾病的潜在治疗作用。
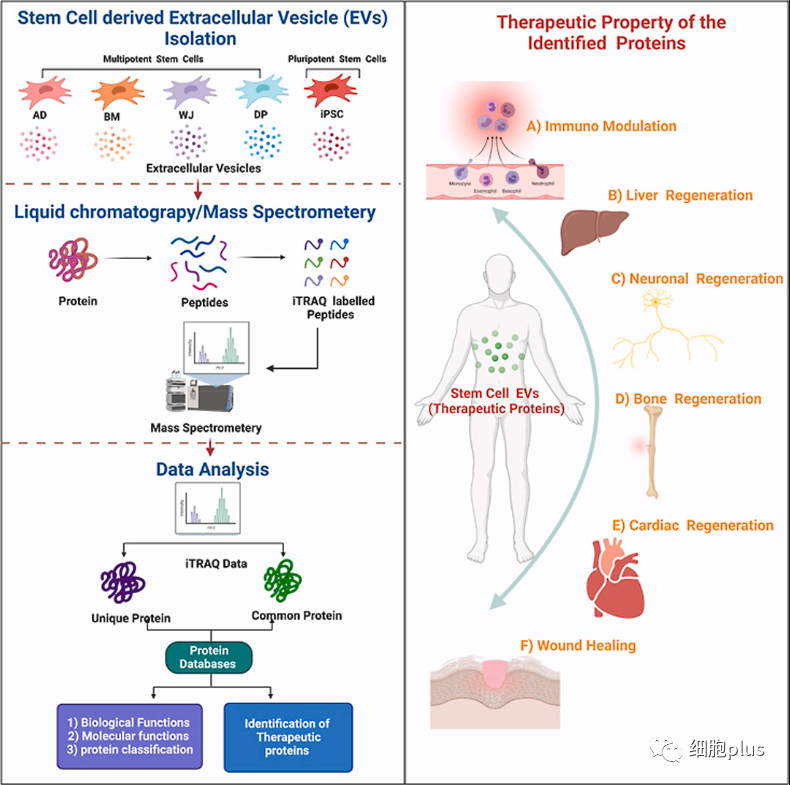
文中研究人员使用iTRAQ(稳定同位素标记蛋白质组学技术)对来自iPSCs和各种组织特异性MSCs(骨髓间充质干细胞 (BM-MSC)、脂肪间充质干细胞(AD-MSC)、脐带间充质干细胞(UC-MSC)和牙髓间充质干细胞(DP-MSC) )的外泌体进行全面定量评价。
生物信息学分析显示在这些外泌体中有223个差异表达的蛋白质。
其中脐带间充质干细胞外泌体包含更多的专有蛋白质,具有更高的蛋白质表达水平。
间充质干细胞外泌体独有113种蛋白质,而其他蛋白质为MSC-EVs和iPSC-EVs共有。
此外,基于对蛋白质、它们的相关途径以及蛋白质间相互作用的深入研究,确定这些蛋白质参与了骨增生(9.3%),伤口愈合(4.4%),免疫调节(8.9%)、心脏再生(6.6%)、神经再生(8.9%)和肝再生 (3.5%)。
总的来说,该蛋白质组学分析结果表明,来源于MSCs的EVs比iPSCs具有更强的蛋白质表达谱和更高的表达水平。
应该说这是一个重要也很基础的发现,特别对于进行iPSCs药物的研发和投资者而言,如果你开发的iPSCs只是通过外泌体起作用的话,恐怕需要更多的调研和斟酌了 。
编辑:小果果,转载请注明出处:https://www.cells88.com/zixun/hydt/18033.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫