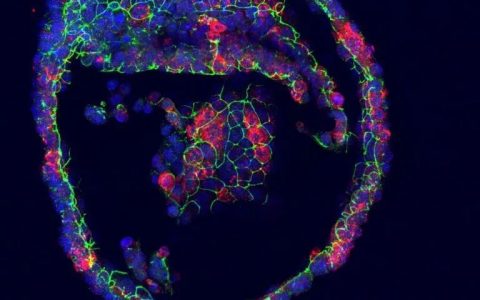
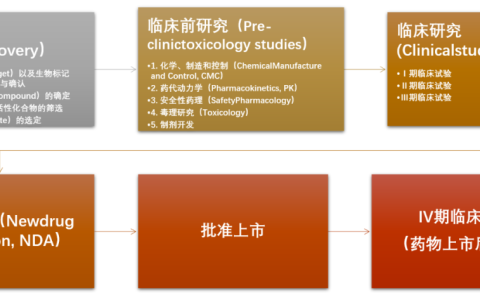
▉ 摘要
关键词:肝癌,炎症,微环境,代谢

https://www.nature.com/articles/s41568-021-00383-9
1. 健康的肝脏微环境
1.1 肝脏的免疫抑制倾向
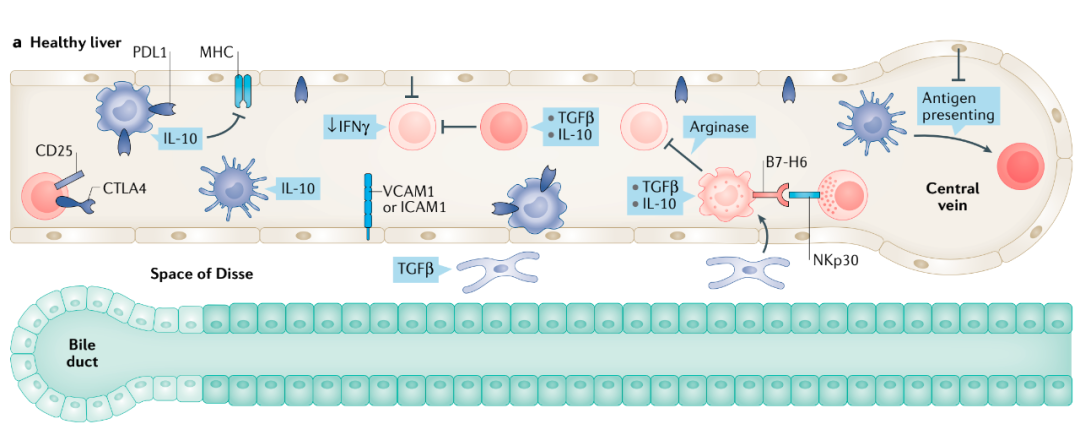
HSCs通过产生抗炎因子如转化生长因子β(TGF-β)促进肝脏发挥免疫抑制作用,从而激活组织再生通路,并激发炎性单核细胞向骨髓源性抑制细胞(MDSCs)分化。
小鼠肝脏中,NK细胞有两种亚型:常规NK细胞(不表达CD49a但表达DX5)和肝脏特异性 NK细胞(表达CD49a但不表达DX5)。特异性NK细胞类似于经典记忆细胞,表达高水平的IFNγ。
Treg细胞是一类控制自身免疫反应性的T细胞亚群,分泌抗炎因子(如TGFβ和IL-10),发挥免疫抑制特性。
LSECs表达PDL1、分子识别受体和粘附分子1(如细胞内粘附分子ICAM1)和血管细胞粘附分子(VCAM1),调节淋巴组织渗透性和MHC Ι类和ΙΙ类。
由于细胞膜完整性缺失,死亡的肝细胞释放出大量与损伤相关的分子。这些“内源性抗原”与过量酒精或脂肪酸分解代谢的产物和异常代谢物,使平衡的免疫耐受性崩溃。KCs最先做出反应,激活受体识别通路,产生大量的促炎因子(如IL-1、IL-6 、TNF、CCL1、CCL2 和 CCL5),上调细胞粘附因子ICAM1和VCAM1的表达水平,下调LSECs上募集单核细胞、中性粒细胞和血小板的PECAM1的表达水平。
固有的先天免疫细胞激活后,适应性免疫细胞和炎症细胞继而被激活(图2)。在NASH小鼠和NASH患者中检测到CD4+和CD8+T细胞的积累。有研究证明,CD4+T细胞促进IFN-γ分泌,从而促进肝脏炎症;CD8+T细胞的免疫消耗可促进NASH诱导的肝脏损伤。
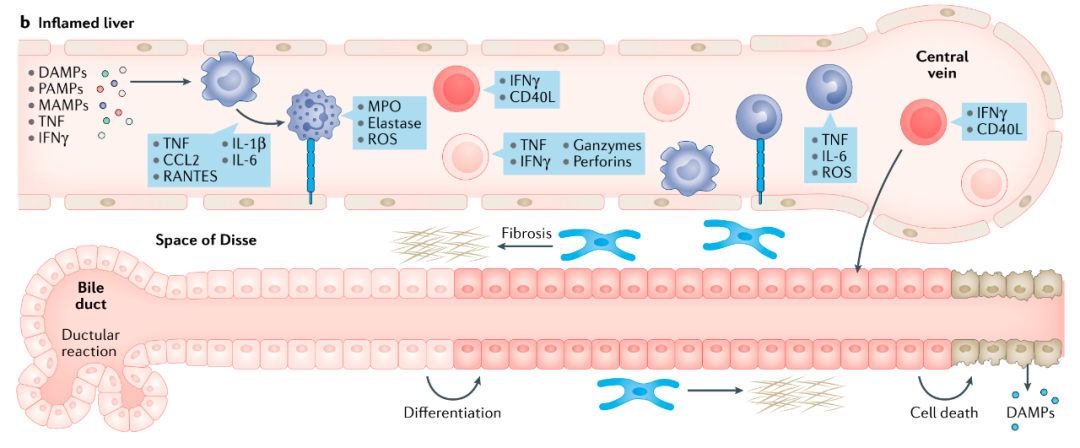
图2 肝脏炎症引起的免疫反应 在炎症性肝病的进展过程中,炎症或代谢异常促进肝脏应激部位固有免疫反应(例如,Kuppfer细胞的激活,中性粒细胞、树突状细胞(DCs)和单核细胞的招募)和适应性免疫反应的激活。免疫激活进一步破坏肝细胞稳态,引起肝细胞循环、肝星状细胞激活和肝窦内皮细胞(LSECs)黏附分子表达,进而引发肝炎。
1.3 肝脏代谢微环境
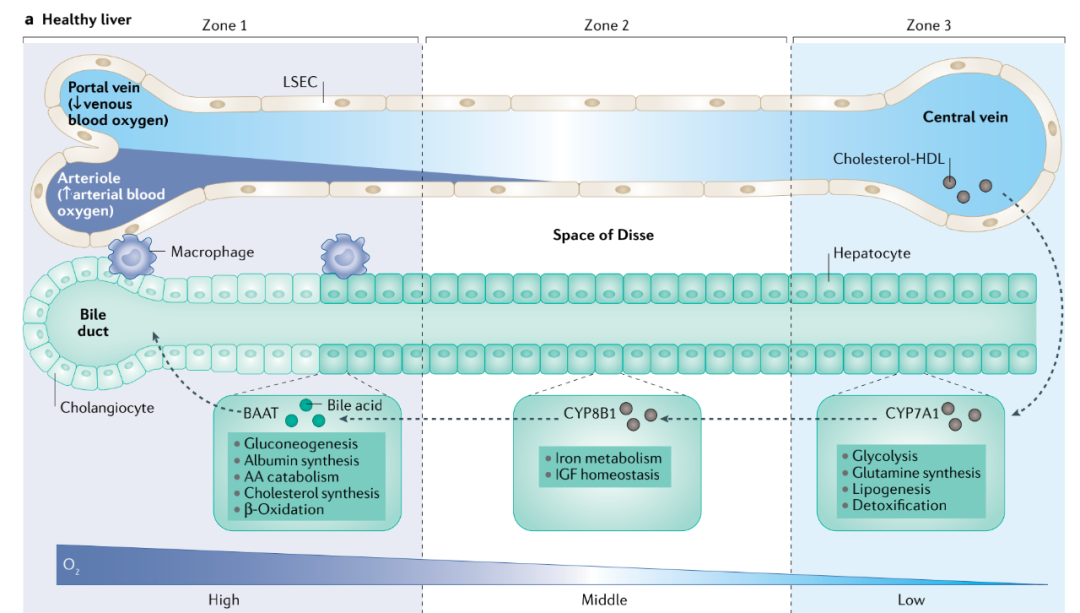
图3 健康肝组织的结构和功能 肝细胞沿空间结构和氧浓度梯度完成新陈代谢、合成、解毒功能,这些功能是根据能量需求即氧含量来划分的。
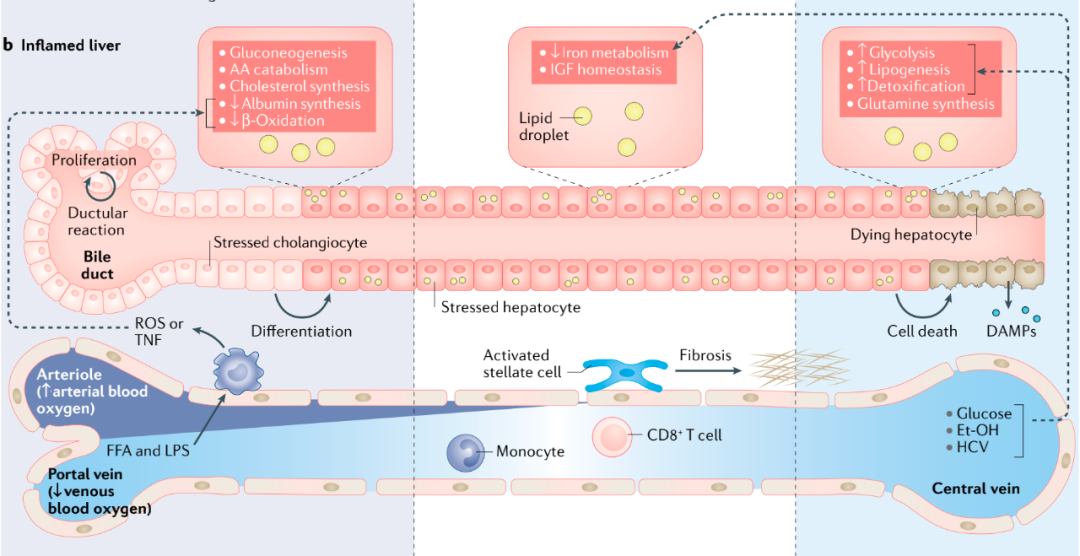
图4 肝脏代谢微环境在病理条件下会发生特定的改变,并发展成癌症。代谢微环境的破坏激活先天免疫反应,进而维持炎症过程。这些变化又导致肝细胞的代谢适应,在慢性坏死性炎症的背景下,导致形成癌前期特征并经历代谢重排。箭头表示代谢物及其中间体在肝小叶的不同区域的运输。
2.1促进癌症发生的炎症通路
炎症引起的细胞死亡和增殖引起氧化应激,进而引起肝细胞DNA损伤和基因突变。8-氧-7,8-二氢-20-脱氧鸟苷和8-硝基鸟嘌呤,诱发ROS和活性氮积累,抑制DNA修复机制中的关键酶,并进一步提高突变率。在氧化应激环境下,细胞癌基因的激活和细胞融合诱导肝细胞衰老。如果没有遗传和免疫监测系统的有效消除,这些衰老细胞就具有癌变潜能。
2.2 肝癌环境下的代谢情况
在NASH和ASH诱导的肝癌中,代谢重排机制至关重要,代谢底物的改变一方面可以增强肝细胞的增殖能力,另一方面还能改变免疫活性。代谢重排机制包括脂质摄入失衡和外周脂肪组织的脂肪酸动员,产生高水平的脂肪酸和葡萄糖,最终诱导癌细胞适应葡萄糖和脂质分解代谢作为主要的能量来源。这种代谢重排不仅使肝癌细胞具有强大的增殖和扩散能力,而且使其容易对化疗药物产生抗性。
代谢环境可以改变肝脏中的免疫反应,使肿瘤细胞发生免疫逃逸(图5)。此外,免疫细胞的代谢重排能引起自身功能异常。肝癌微环境中的巨噬细胞发生M2极化,这种表型与脂肪酸氧化能力的增强和肿瘤细胞迁移有关。代谢重排还会影响T细胞的抗肿瘤活性,在HCC微环境中,Treg细胞的增多与它们利用含能底物(如脂类和葡萄糖)的能力有关。在肿瘤微环境中,促炎免疫细胞的有氧糖酵解速率增加。
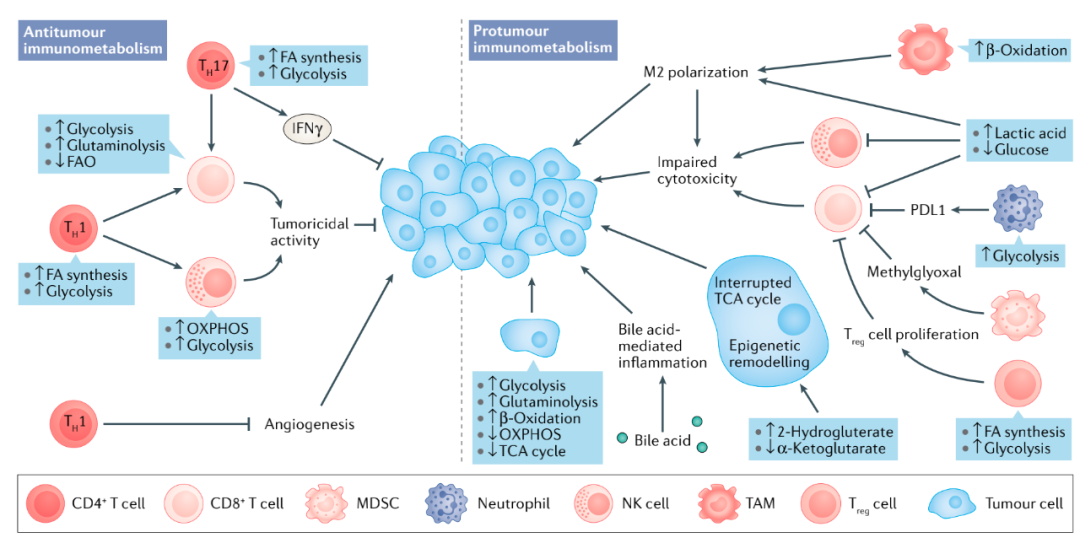
图5 肝癌条件下的免疫微环境 在肝癌中,代谢重排通过支持癌细胞和肿瘤免疫微环境的能量需求在疾病的进展中起着核心作用。肿瘤细胞上调糖酵解、糖异生和β-氧化来支持快速增殖,导致葡萄糖缺乏和乳酸丰富的微环境。
3 肿瘤的监督途径
3.1 基因监督
3.2免疫监督
NK细胞和自然杀伤T细胞是另一免疫监督机制。肝癌患者外周血和瘤内组织中的肿瘤浸润NK细胞数量减少,并且在细胞因子生成和细胞毒性方面功能受损。自然杀伤T细胞产生IFN-γ且激活NK细胞,抑制肿瘤生长。
炎症相关的巨噬细胞和单核细胞具有抗肿瘤作用。在肿瘤微环境中,这些细胞被称为肿瘤相关巨噬细胞,具有免疫抑制表型,并通过组织重塑(如血管生成和伤痕修复)促进肿瘤进展和转移。
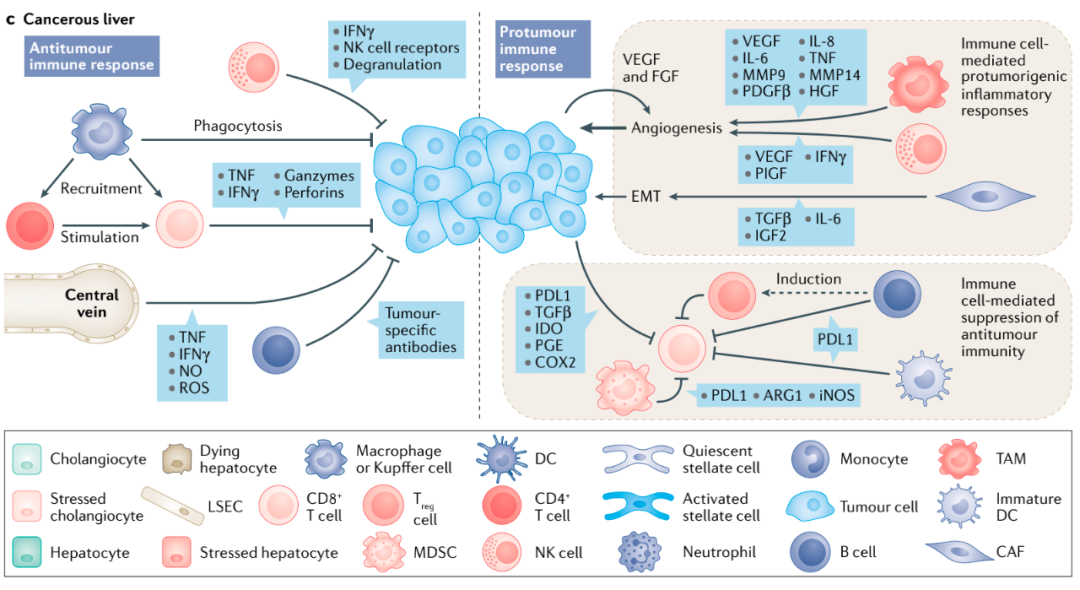
图6癌变肝脏组织 LSECs 分泌IFN-γ、 一氧化氮(NO)和活性氧(ROS) 杀死肿瘤细胞;Kuppfer细胞通过吞噬作用和募集T细胞产生抗肿瘤免疫反应;自然杀伤细胞(NK)也参与抗肿瘤免疫反应。
4. 展望
尽管我们对肝癌的起源和分子特征的认识取得了巨大的进步,但能够显著提高患者生存率和改善患者生活质量的治疗方案仍然很少。最近,PDL1抑制剂atezolizumab联合抗VEGF药物bevacizumab获得批准,一种新的治疗晚期肝癌的标准疗法成功实施。最新的数据表明,这种联合免疫疗法对病毒诱导的肝癌能起到有效地免疫监测。相比之下,非病毒型肝癌限制了免疫疗法触发的免疫监视的功效。
因此,靶向治疗和重塑肝脏炎症和代谢微环境,以及更好地理解和精确靶向血管生成、纤维化和营养供应,能够增强肿瘤的淋巴细胞浸润,重新建立有效的免疫监测和免疫检查点封锁反应。
编辑:小果果,转载请注明出处:https://www.cells88.com/linchuang/lcyj/10300.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫