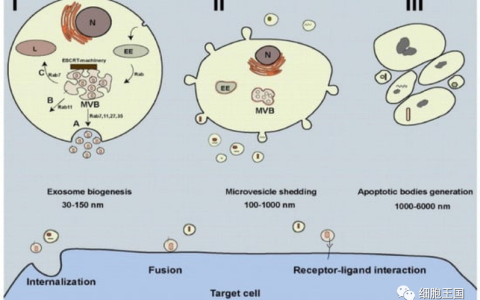
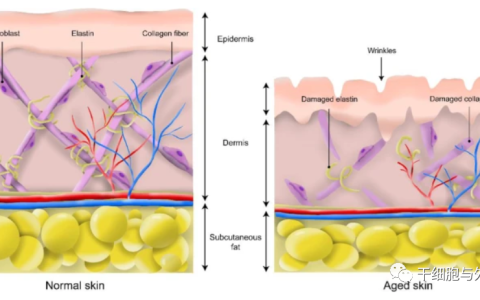
在2022-2027年的预测期内,外泌体市场预计将以27.89%的复合年增长率增长。
推动干细胞外泌体市场增长的因素包括新冠的流行、干细胞技术的发展和政策限制、外泌体分离和分析程序的技术进步以及外泌体的应用场景不断增加。
然而,要在各种应用中成功实施外泌体,还需要解决许多技术难题。
这里面包括对外泌体的优化纯化、保持外泌体的同质性和高效的转染策略,其中分离/纯化方法的繁琐以及对外泌体和免疫系统交互作用了解不完全都限制了外泌体市场的发展进程。
其他因素还包括对外泌体产品的批准和商业化的严格监管要求。
因此,截止目前只有少数公司如Aegle Therapeutics、Exopharm Ltd、United Therapeutics、Avalon Globocare、Organicell和Direct Biologics,突破了将干细胞外泌体带向临床的关键瓶颈。

2018年5月11日,Aegle Therapeutics宣布,FDA已经批准了其间充质干细胞外泌体AGLE-102产品的第一个IND申请,以启动对严重二度烧伤患者的外泌体临床试验。该公司于2018年底启动了该产品的1/2a期试验,使Aegle成为第一家获得FDA批准进入人类临床试验的细胞外囊泡(EV)公司。
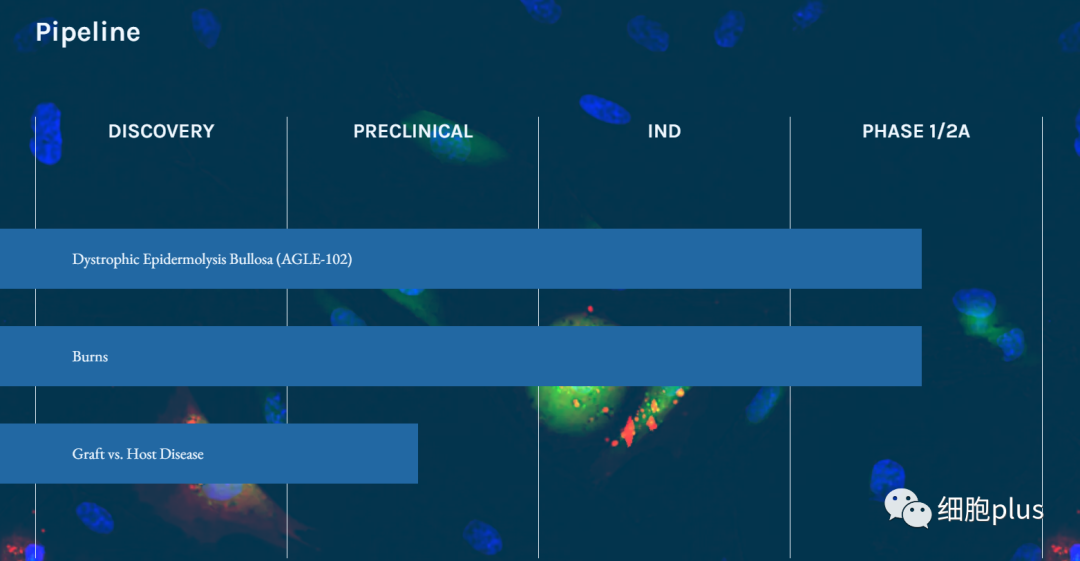
2019年5月20日,该公司又宣布其AGLE-102产品治疗营养不良性大疱性表皮松解症获得FDA批准进入临床试验。

2020年1月28日,总部位于墨尔本的Exopharm宣布了其人类临床试验的首次给药,成为第一家应用外泌体治疗伤口愈合的公司。其I期研究正在测试Exopharm的Plexaris产品,这是一种来自血小板外泌体的无细胞制剂,在临床前动物研究中显示出再生效果,改善伤口闭合并减少疤痕。

2019年6月,United Therapeutics宣布批准对支气管肺发育不良(BDP)进行基于外泌体的治疗的I期试验,这种疾病在接受辅助通气和补充氧气的早产儿中很常见。BDP的特点是肺部生长和发育受阻,对健康的影响会持续到成年。

Organicell正在开发Zofin,这是一种源自围产期来源的无细胞生物治疗药物,旨在保留自然产生的外泌体。
Organicell已收到美国FDA针对Zofin治疗新冠肺炎的18份eINDs(紧急ind )。

美国FDA还批准了Organicell进行四项I/II期随机安慰剂对照试验,研究Zofin对慢性阻塞性肺病(COPD)、骨关节炎(OA)、新冠肺炎和COVID Long Haulers的治疗潜力,以及一项针对轻度至中度新冠肺炎的扩大准入试验。
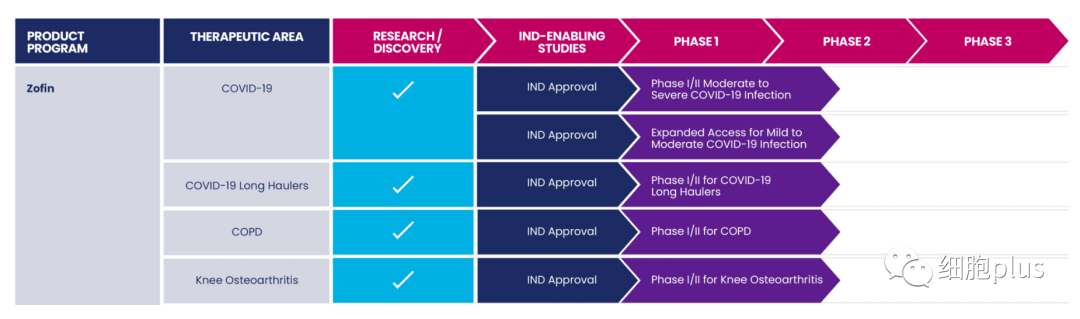

美国FDA批准Direct Biologics的一项IND临床试验,同意其将骨髓间充质干细胞外泌体ExoFlo产品用于治疗新冠肺炎诱发的ARDS。
Direct Biologics是唯一一家IND批准用于所有新冠肺炎适应症(包括ARDS)的外泌体公司。
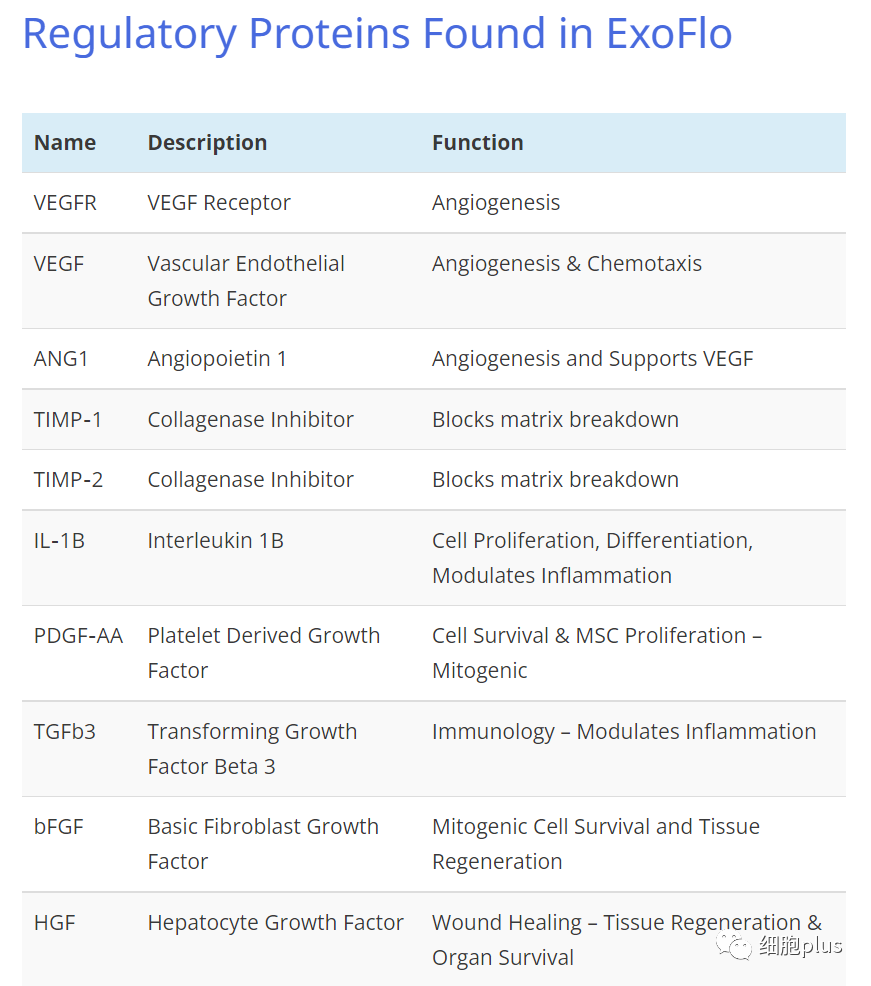
Direct Biologics目前正在进行一项多中心、随机临床试验,以研究其ExoFlo胞外囊泡产品。最近,它宣布美国食品和药物管理局已授权它扩大其正在进行的ExoFlo的3期临床试验全因中重度急性呼吸窘迫综合征。

Evox Therapeutics开发了7种基于外泌体的候选治疗产品。其候选药物有可能解决溶酶体贮积症(LSD),该病全球发病率接近1/5000,以及一些遗传病包括先天性代谢缺陷(IEM)。
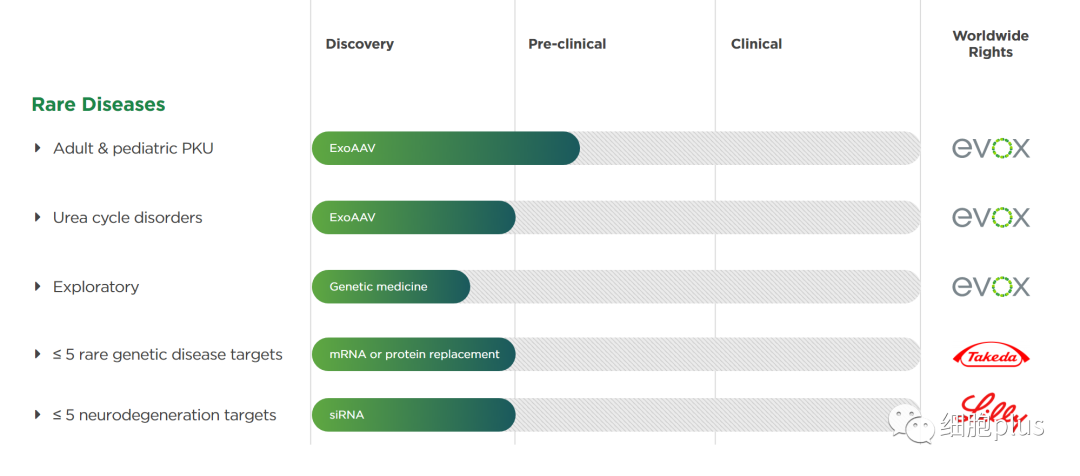
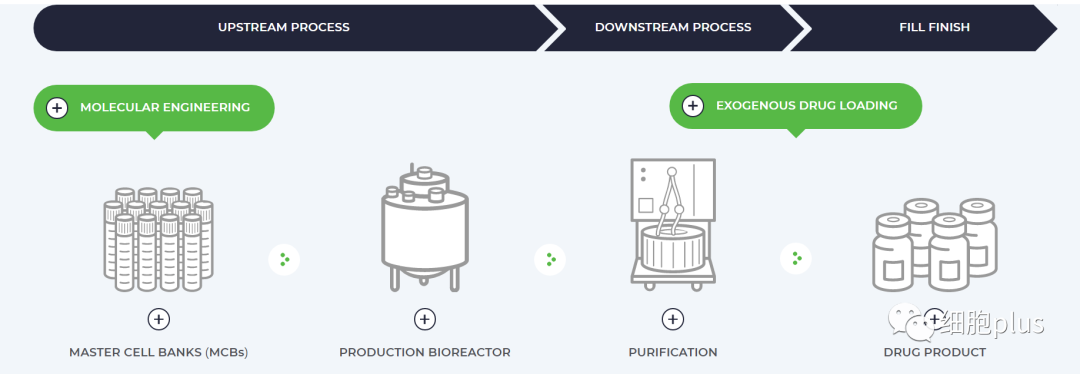
该公司的技术主要是将药物和组织靶向蛋白装载到外泌体的表面。


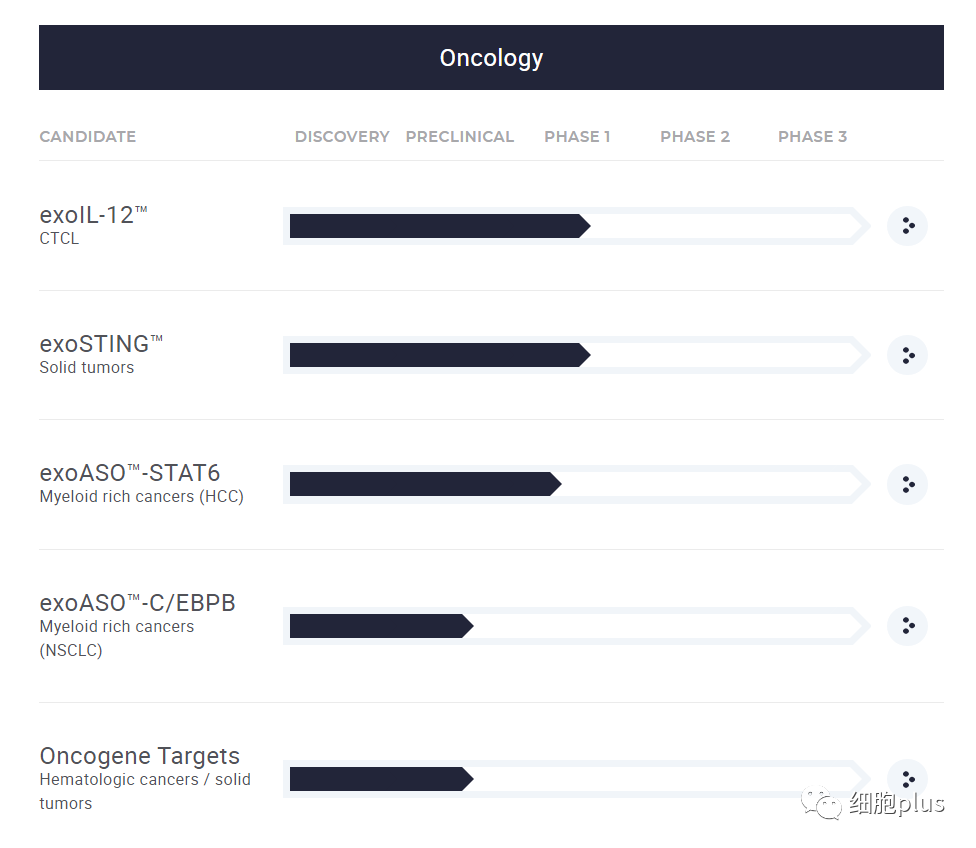
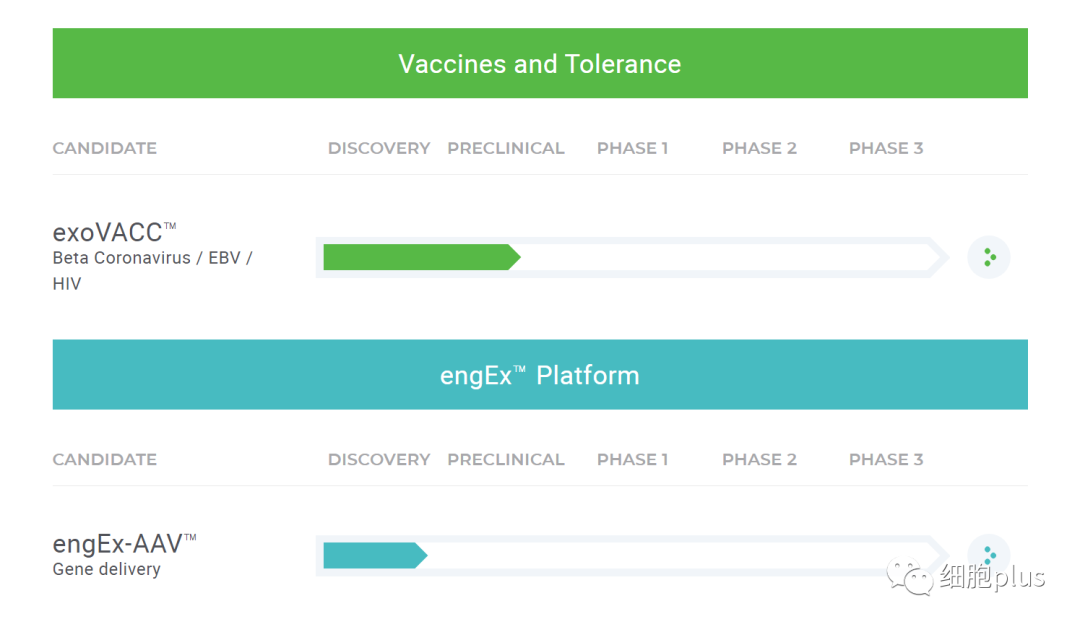
Codiak BioSciences的产品线包括各种治疗领域的多个候选产品。
其engEx平台专注于工程外泌体,以针对免疫疾病、代谢和纤维化疾病、神经退行性疾病、癌症和罕见疾病。

独辟蹊径的公司也有,譬如Aethlon Medical采取一种不同的方法——出于治疗目的去除外泌体。
Aethlon开发了一种治疗性血液滤过技术,通过亲和吸附来捕捉和清除循环病毒和促癌外泌体。它的血液净化装置正在接受FDA备案的临床研究评估。

Aethlon还是Exosome Sciences公司的大股东(80%),该公司主要研究用于诊断癌症和神经疾病进展的外泌体生物标记。
在初步研究中,公司的ELLSA平台展示了从尿液中分离外泌体的能力,从而实现了对HIV感染的高灵敏度检测。
针对神经系统疾病,Exosome Sciences发现了TauSome,这是一种体外生物标记物,可能是第一个检测活体个体慢性创伤性脑病(CTE)的非侵入性候选物。在一项对前国家橄榄球联盟(NFL)球员的研究中,发现与参加非接触运动的运动员对照组相比,橄榄球运动员TauSome水平明显更高。TauSome水平也与基于记忆和精神运动速度标准化测试的认知下降相关。
外泌体疗法的商业化前景
我们已经看到了干细胞外泌体庞大的商业版图和众多跃跃欲试的公司,就差捅破最后一层薄薄的纸,不过希望就在眼前,当前处于III期和IV期试验的五种外泌体候选产品有望在不久的将来获得市场批准。
而两种应用外泌体技术的诊断测试,即用于前列腺癌的ExoDx Prostate(IntelliScore)和用于非小细胞肺癌的Guardant 360 CDx,已经获得美国FDA的批准,并已上市。
外泌体科学研究和临床试验的比率也在上升,这表明外泌体疗法有着光明的前景。
总的来说,全球至少有118家公司正在开发各种各样的外泌体疗法、诊断、研究产品和制造技术。
编辑:小果果,转载请注明出处:https://www.cells88.com/cells/wmt/32215.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫