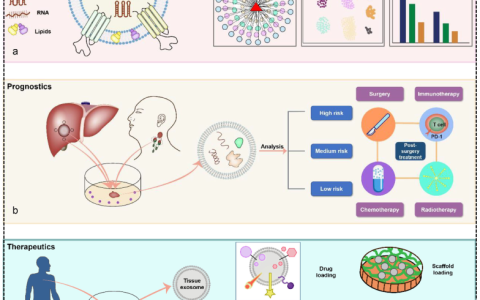
与细胞外囊泡(EV)相关的不同来源、纳米级和侵入性分离程序意味着它们通常被大量研究并与其亲代细胞断开关联。近日,来自英国曼彻斯特大学的研究人员在JEV杂志上发表文章,使用超分辨率显微镜直接比较单个人类单核细胞衍生巨噬细胞(MDM)分泌的EVs。研究发现不同类型巨噬细胞分泌的EVs特征(大小、携带的蛋白)不同。超分辨率显微镜可以在单个细胞的基础上对EV进行定量分类,以根据其EV分泌物定义巨噬细胞亚群。

巨噬细胞存在于全身组织中,它们在先天免疫和适应性免疫的协调中发挥关键作用。它们有能力对许多环境刺激做出反应,这些刺激会导致不同的激活状态,从而实现专门的功能。虽然巨噬细胞表型高度异质,但有两种主要的活化表型;经典激活的M1巨噬细胞和交替激活的M2巨噬细胞。此外,M0用于描述预激活的巨噬细胞。M1巨噬细胞通常是促炎细胞,而M2则表现出更再生的表型。除了M1和M2巨噬细胞外,环境因素会导致进一步的特化,例如肺泡巨噬细胞和肝脏中具有可变M1和M2表型的Kupffer细胞。
巨噬细胞在免疫反应中具有多种作用。用IgG介导的外来颗粒的检测和吞噬作用通过Fcγ受体(FcγRs)的连接发生,该受体触发细胞活化、吞噬作用和炎症介质的释放。在遇到识别过的颗粒时,巨噬细胞会在吞噬其目标之前形成吞噬突触。除了直接吞噬病原体外,巨噬细胞还通过形成免疫突触与适应性免疫系统的细胞相互作用,与吞噬突触类似,这些突触是细胞信号传导的结构化区域。病原体衍生的抗原可以通过MHCII类蛋白在巨噬细胞-T细胞界面呈递给T细胞受体(TCR),从而导致T细胞活化。此外,巨噬细胞分泌细胞因子和细胞外囊泡(EV),它们可以启动T细胞并以多种方式调节免疫反应。抗原呈递和细胞因子释放是经过充分研究的方式,巨噬细胞通过这些方式调节免疫系统的激活和分化。然而,直到最近,EVs还没有得到充分研究,并被认为是一种废物清除机制,而不是细胞间通讯和受体细胞功能调节所必需的。
已经确定了多种EV亚型,例如外泌体、微泡和凋亡小体,这些亚型可以通过它们的起源和大小来表征。EV的作用可以是生理和病理的,取决于它们的货物和膜组成。Tkach等人证明来自未成熟树突状细胞的小型和大型EV差异诱导CD4+T细胞活化,巨噬细胞衍生的EV已被证明会影响其他细胞的功能。例如,LPS诱导的肺泡巨噬细胞分泌EV可促进ICAM-1在上皮细胞上的表达。
尽管取得了很大进展,但我们对EV亚群的异质性和多样化功能的理解仍处于起步阶段。事实证明,了解EV的细微差别具有挑战性,因为EV几乎完全是批量研究的,这只能揭示整个EV群的平均影响。因此,这些研究提供的关于EV组成、大小和货物的异质性及其细胞间变异性的信息有限。一种更深入地了解单个EV的方法是超分辨率显微镜,它已被用于识别孤立EV中胰腺癌的生物标志物,并跟踪癌症衍生EV的细胞间转移。然而,尽管这些研究表明了超分辨率显微镜在EV研究中的潜力,但这些研究仍然将EV与产生它们的单个细胞断开,因此无法理解单细胞分泌物的贡献和异质性。
该研究利用超分辨率显微镜直接观察和表征单个巨噬细胞分泌的EV的异质性,并揭示HLA-DR在M1样肺巨噬细胞衍生的EV上显著富集。定量单细胞分泌谱分析使我们能够根据它们分泌的EV将单个巨噬细胞分为五种亚型。为由低M0和M2样EV分泌谱非常相似,但分或非常低HLA-DR表达定义的两种类型。从单个肺巨噬细胞释放的EV形成两种富含HLA-DR的类型,大约20%的M1样巨噬细胞分泌与肺巨噬细胞匹配的EV。其他M1样细胞表现出第五种分泌亚型。因此,超分辨率显微镜可以在单个细胞的基础上对EV进行定量分类,以根据其EV分泌物定义巨噬细胞亚群。
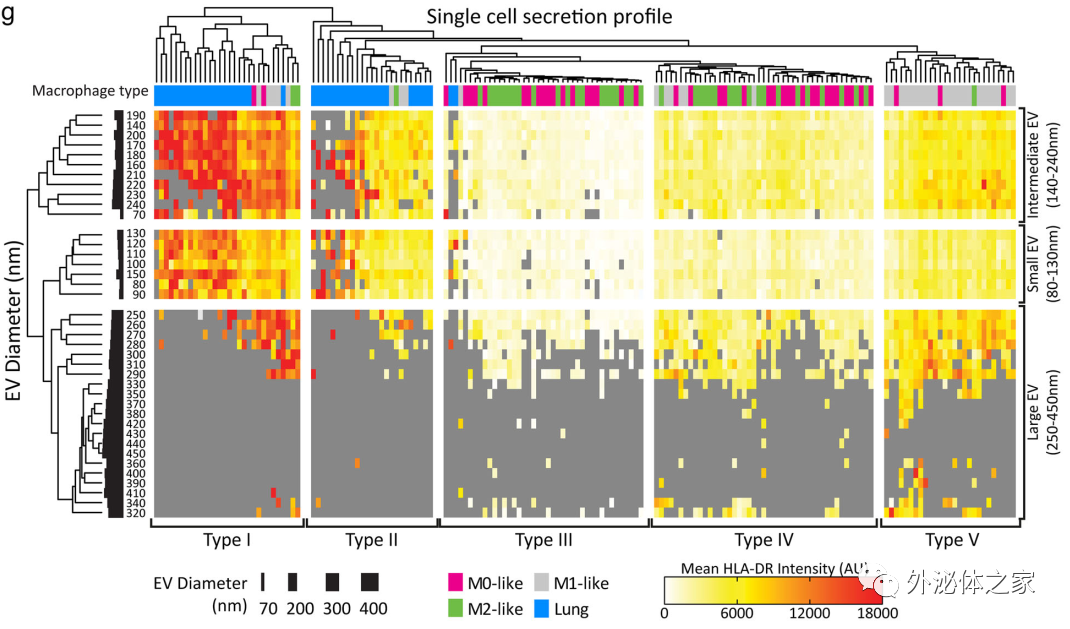
比较单个巨噬细胞的EV谱
MDM被区分为M0、M1或M2样,激活后所有三种分泌EV的密度相似。然而,M0样细胞比M1和M2样巨噬细胞分泌更大的EV。蛋白质组学分析揭示了不同大小的EV的成分以及不同MDM表型分泌的EV之间的差异。单细胞分泌物的超分辨率显微镜发现II类MHC蛋白HLA-DR在约40%的M1样MDM分泌的EV上表达,这是M0样和M2样EV观察到的频率的两倍。从癌症患者切除的肺中分离出的人类巨噬细胞分泌的EVs表达HLA-DR的频率是M1样EVs的两倍,强度更高。对所有四种巨噬细胞表型的单细胞EV谱的定量分析揭示了不同的分泌类型,其中五种在多个样本队列中是一致的。M1样MDM的一个亚群分泌与肺巨噬细胞相似的EV,这表明在癌症患者的肺部内具有特定EV分泌谱的细胞的扩增或募集。因此,EV异质性的定量分析可用于单细胞分析和揭示新的巨噬细胞生物学。
参考文献:
DechantsreiterS, Ambrose AR, Worboys JD, Lim JME, Liu S, Shah R, Montero MA, Quinn AM,Hussell T, Tannahill GM, Davis DM. Heterogeneity in extracellular vesiclesecretion by single human macrophages revealed by super-resolution microscopy.J Extracell Vesicles. 2022 Apr;11(4):e12215. doi: 10.1002/jev2.12215. PMID:35415881; PMCID: PMC9006015.
编辑:小果果,转载请注明出处:https://www.cells88.com/cells/wmt/12343.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫