01
介绍
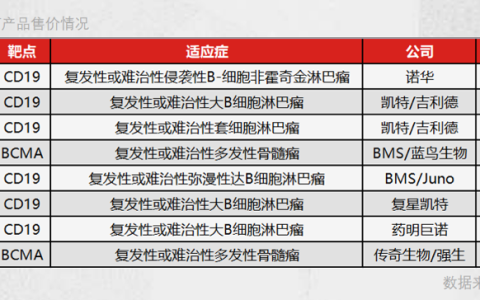
最近,FDA 批准了几种 CAR T 细胞治疗药物,第一个是tisagenleucel(商业名称Kymriah™),于 2017 年底用于治疗难治性B细胞前体急性淋巴细胞白血病。紧随其后的是用于治疗大B细胞淋巴瘤的 axicabtagene ciloleucel (Yescarta™),后来又出现了其他药物,例如brexucabtagene autoleucel(Tecar tus™)对抗套细胞淋巴瘤。
过去几十年开发的扩展程序为I/II期发展研究带来了出色的结果,特别是,使用生物反应器是一种用于过继转移T细胞体外培养的有前途的方法。生物反应器被定义为在受控环境中装有细胞、其他生物体和/或生物活性物质的容器:仔细监测温度、营养物质、废物、pH、机械要求和流速以实现多种生物技术过程(图 1)。开发了许多生物反应器设计来满足这些不同研究领域的特定要求。
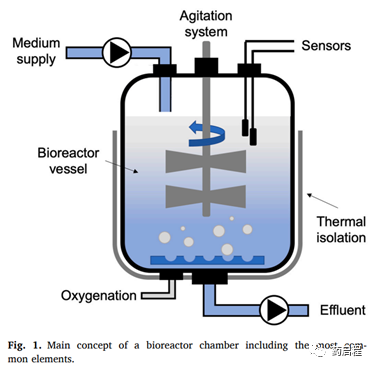
生物反应器的方法仍处于起步阶段,过去10年的文章数量似乎达到了平台期(图 2)。这一现象凸显了对新方法、发现和优化的迫切需求,以进一步实现基于生物反应器系统的临床规模生产。
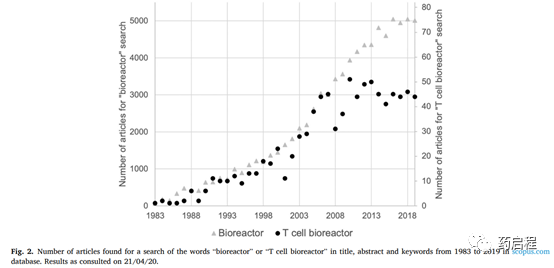
在本文中,首先介绍了对T细胞培养和治疗的一般考虑,包括对除扩增之外的其他步骤的简要概述。然后讨论了特定的T细胞培养要求,以强调指导新扩增过程开发的主要目标和方法。最后,报告了当前的黄金标准,即培养瓶和移动培养袋,并与主要的生物反应器设计进行了比较,即中空纤维、袋式生物反应器和改进的烧瓶系统,以及原始和最近的建议。
02
T细胞的一般考虑
有一系列方法可用于在T细胞过继转移后产生强大的治疗作用。用于细胞治疗的TIL制造通常需要标准的体外扩增步骤:TILs从肿瘤活检中分离、洗涤和浓缩,然后扩增至临床相关的回输规模。然而,TIL并不总是自然存在,只能从某些患者身上产生。因此,已经开发了基于T细胞受体 (TCR) 或嵌合抗原受体 (CAR) 的其他策略。
通过这种方法,来自患有其他癌症的患者的正常T细胞通过单采分离并转导以产生TCR或CAR T细胞(图 3)。
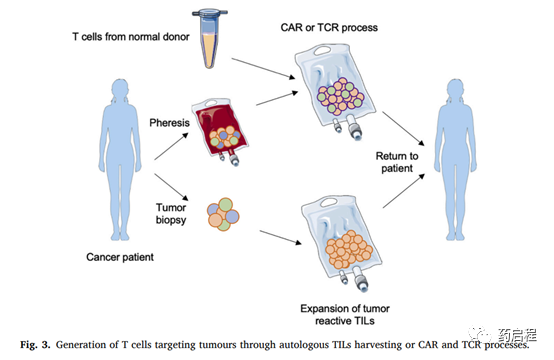
必须执行激活程序以允许制造的T细胞的转导和增殖。T细胞激活和增殖的完整环境包括抗CD3抗体和外源性IL-2,以及作为饲养细胞的外周血单核细胞。这种组合被报告为标准的“快速扩展协议”(REP)今天仍在研究如何改进和完善REP,例如使用额外的培养基补体(IL-7、IL-15、抗 CD28 抗体)以及使用专注于pp65蛋白的肽混合物进行预刺激,导致在同一培养容器中获得更高的增殖率。
由于记忆T细胞,为了在快速移植、抗肿瘤活性和长期保护方面获得最佳结果,已经表明需要大部分CD8+,但有一些CD4+ 细胞高于阈值(经典培养条件下的研究) 以及如下所述的Wave系统。此外,有人认为CD4+ T细胞在体内更有效:CD4+ T细胞与 CD8+ T细胞具有相同的细胞毒活性;然而,CD4+子集在TCR参与后更加持久。用于治疗的最有效T细胞亚群尚未确定。
所使用的抗体对产生的 T 细胞的治疗质量也有很大影响。与CD28共刺激相比,表达4-1BB的基于细胞的人工抗原呈递细胞增加了CD8+T细胞的扩增。
由于T细胞活化涉及许多因素,很明显,任何涉及活化步骤的生物反应器都应评估其对T细胞与抗原呈递相互作用的影响。例如,搅拌以改善生物反应器中的传质可能会显着影响T细胞活化。
尽管出现了此类标准化程序,但仍在研究基于专用培养系统的更复杂环境,以获得最佳增殖,从而产生足够的TIL或TCR/CAR细胞用于治疗。为了更进一步,必须了解该谱系的培养要求、持续的挑战以及生物反应器扩展的具体目标。
03
生物反应器扩增的好处
3.1.细胞数
如前所述,开发用于培养T细胞的生物反应器系统的主要目标是与静态烧瓶培养相比,进一步提高体外增殖率,超越REP和激活步骤。分离细胞的数量仍然太少,无法确保有效的自体免疫治疗。在儿科和年轻成人CAR T试验中,开发了一种复杂的算法和方法,以实现预期的32.4亿CD3+T细胞单采。对于最终的治疗产品,大多数研究报告称一名患者需要1-1000亿个细胞。
在本文中,将讨论在特定类型的设备中可以实现的最大细胞密度和最大产量。然而,必须注意的是,系统之间的设计和功能差异,例如中空纤维生物反应器和搅拌罐系统,使得在不考虑所有其他特征和参数的情况下很难或几乎不可能严格比较最大细胞密度。因此,在评估生物反应器在T细胞应用中的潜力时,它不应该是唯一要考虑的参数。
3.2.降低成本和数量
增殖率的提高将有助于减少溶液量和劳动时间,进而减少细胞疗法的成本。事实上,T 细胞扩增通常在经典条件下持续14天和由于细胞密度低,可能需要数十升培养基才能获得所需数量。因此,优化生物反应器设计以减少体积并改进T细胞培养物的补料计划以在营养支持、废物去除和培养基成本之间找到平衡至关重要。
此外,已经表明部分培养基改变可以改善细胞扩增,因为完全改变导致去除所有有益的自分泌因子,如干扰素-γ、IL 1β和肿瘤坏死因子-α,导致增殖减少。然而,相反,开发复杂的生物反应器系统可能会增加采购和启动成本,特别是对于参与设计和优化早期步骤的小型学术结构。因此,在评估生物反应器的经济利益时,需要仔细考虑这种平衡。
3.3.促进符合良好生产规范 (GMP) 的协议
由于当前 T 细胞扩增方案的高劳动强度,促进确保GMP的过程非常重要。如前所述,减少体积和培养步骤对此类方法以及自动化有积极贡献常规程序和封闭系统的使用。生物反应器的设计应避免细胞群在扩增期间多次暴露于外部环境,用于进料和取样以及从一个培养系统转移到另一个培养系统消除了对洁净室等大型设施的需求。GMP还应应用于初始和辅助步骤,例如 TCR/CAR 细胞的冷冻保存或转导过程,从而促进将研究转化为临床试验。
04 生物反应器系统
4.1.基于中空纤维膜的生物反应器:Terumo Quantum
首先中空纤维滤芯在40多年前开发用于透析系统(图 4A),后来被提议用于细胞培养和进一步应用并最终成为生物反应器。早些年,中空纤维中的一些T细胞相关研究并不关注细胞扩增。中空纤维创造了一个两室培养环境,因为细胞在小中空纤维(直径200μm)的一侧生长,而培养基在另一侧灌注(图.4B)。纤维由可渗透特定目标成分(生物分子、气体、营养物质、废物)的膜制成,因此允许细胞隔室和培养基灌注之间的受控交换。
将此类系统应用于T细胞培养的基本原理是由于分隔几何结构,避免了由流动灌注引起的剪切应力,同时保持介质运动,如在摇袋和搅拌罐中,有机会重新充氧并调节培养基pH值,然后再将其送回细胞。此外,细胞室中培养基的闭环和营养物质的浓度有助于减少喂养所需的体积。此处关于细胞密度的方法是在固定体积(细胞室)中增加浓度,但是流速可以随着细胞数量而增加。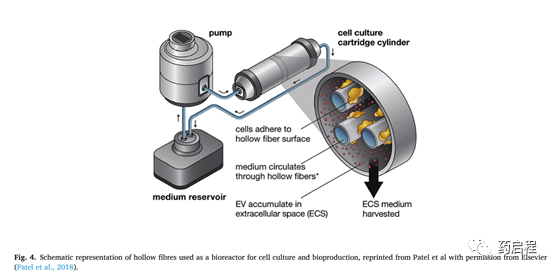
这种系统的一个潜在问题是要提供或去除的分子的大小,尤其是随着细胞密度的增加。T细胞逐渐产生的抑制物的生长必须很容易去除 确保持续增殖和扩张,这可以通过纤维膜实现,如早年所示。以类似的方式,生长因子应该能够反过来从灌注到达细胞区域。因此,扩增所需的T细胞特异性激活因子(即推荐遵循REP的IL-2和抗体)的分子量将指导要使用的膜的选择。例如,特里克特等人。注意到聚丙烯基中空纤维(制造商列出的0.3-0.5μm 膜孔径)比4kDa纤维素滤芯更适合IL-2扩散。
以中空纤维为中心的生物反应器系统的一个商业示例是Terumo Quantum®。该系统能够在系统中的一个一次性使用套件内将T细胞培养到治疗剂量;接种1×10^8个淋巴细胞后,它能够使细胞数量增加 90-500倍。因此,在使用Quantum®系统的实验中,起始细胞数量非常高,并且起始材料质量可能是 T 细胞过继转移的一个挑战。可能需要进一步研究该系统对起始材料参数(如细胞数)变化的适应性,以确认其全部潜力。
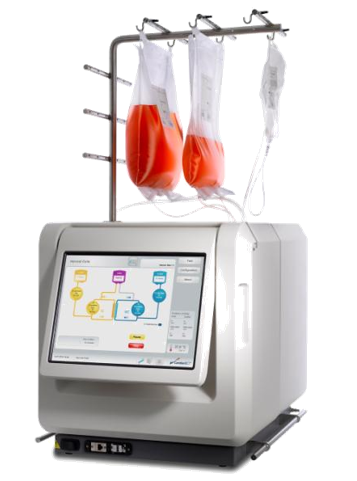
T细胞与称为Dynabeads的聚合物颗粒的共培养经常用于中空纤维、波浪袋和搅拌罐生物反应器形式的活化步骤。对于中空纤维形式,由 T细胞的dynabead激活和Quantum®扩增产生的CD4+:CD8+比率高度依赖于供体材料。大多数样本倾向于促进CD8+细胞的增殖;然而,对于一名捐助者,该比例接近1:1。
改进初始结果,Quantum®系统中的优化方案发现,除了其他参数的变化外,增加每个T细胞的dynabeads数量会导致生物反应器产生更高的倍数扩增。该研究未报告对T细胞表型的影响。关于生物反应器产生的T细胞亚群的结论是,它可能依赖于与生物反应器无关的因素,但例如与供体变异性相关的因素,尽管这些研究缺乏与使用上述金标准方法的对照实验相关的数据.
Quantum® 和中空纤维生物反应器的一个独特之处在于它们能够培养贴壁细胞,因此也可以生产用于转染CAR T疗法的慢病毒载体。
此外,由于中空纤维系统已用于细胞培养以生产细胞分泌产物,因此有良好的行业基础设施来支持该系统,同时承认在培养结束时收获细胞的要求可能会带来一些挑战。
4.2.改进的烧瓶:G-Rex® 系统
常规培养T型烧瓶的优点是易于使用且价格合理。因此,开发更具相关性但易于监测的培养环境的一种方法是设计具有附加功能以提高增殖率的“改进烧瓶”。尽管可以理所当然地讨论此类设备的生物反应器性质,但根据生物反应器的严格定义,它们确实可以被视为具有微控制环境的容器,特别是通过气体交换。
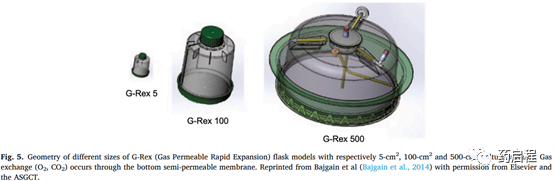
用于透气性快速膨胀的G-Rex®系统大约在10年前由Wilson Wolf Manufacturing开发,作为T型烧瓶、旋转烧瓶和半渗透袋的替代品。该细胞扩增室的主要特征是位于底部的半透膜与主要细胞培养表面区域接触(图 5)。与常规T型烧瓶相比,该容器可以填充非常大容量的培养基,其中限制为1mL/cm2以避免细胞缺氧。该装置已经过悬浮细胞测试,可以与 REP 结合使用,包括添加饲养细胞。因此,它被考虑用于T细胞的扩增。根据制造商的信息,较大的初始体积以及对细胞传代和培养基变化没有特定要求意味着在恒定体积中增加细胞密度以进行 T 细胞扩增。G-Rex® 烧瓶已使用不同的协议作为半开放或封闭系统进行了研究。
4.3.改进的培养袋:波浪生物反应器和GE Xuri系统
Wave生物反应器最初由Singh等人开发。1999年作为替代生物反应器,与以前的系统相比,可以轻松扩大规模。它被提议用于各种应用,例如贴壁和非贴壁细胞培养以及腺病毒生产。然后最近专门研究了T细胞的扩增。
该系统使用无菌一次性培养袋作为平台上的主要容器,确保加热和摇摆运动(可变角度、幅度和速率)以在培养基中诱导“波浪”(图 6)。即使在小体积的高细胞密度下,这些特定的运动也能提供更好的氧交换、均匀性和易于获取营养物质,同时与搅拌系统相比减少了对细胞的压力。培养基可以通过袋子灌注,标准管道端口允许采样和接种。该生物反应器已成功用于 I 期和 II 1期临床试验。因此,与静态和单轴振动袋相比,该系统的主要创新特征是在封闭系统中将复杂的波回路与流动灌注相结合。这种组合即使在细胞尺度上也能提供更好的均质性,因为它避免了位于细胞附近环境中浓度最高的有益分泌因子的梯度。因此这是一个更复杂的 从技术的角度来看,系统比当前的黄金标准要好,但实际上它不会增加劳动时间,因为监测和采样很简单,甚至是自动化的。
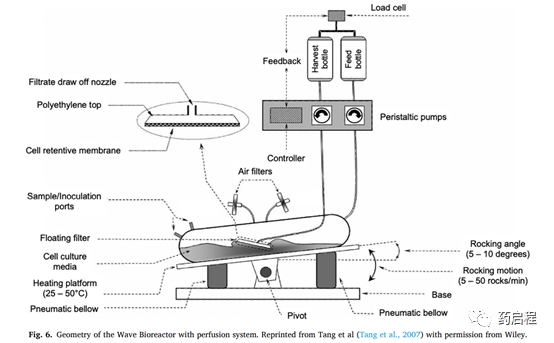
此外,REP 过程的所有步骤都可以直接在系统中进行,而只有 REP 的后期阶段才适合在其他设计中运行,例如基于中空纤维膜的生物反应器。除了增加增殖率外,这种方法还可以通过缩短培养过程来提高标准产量,这要归功于更容易处理和监控。
使用透明培养袋本身就是一个优势,因为它们是一次性的,可以消毒,光学透明,并允许通过培养基进行显微镜观察和非侵入性光学测量。
由于这些特点,Wave 生物反应器已被用于 T 细胞扩增,采用恒定体积和增加细胞密度的方法,结合流动灌注,其方式与中空纤维生物反应器类似.然而,由于单独的摇摆运动提供了混合和氧气交换,因此可以研究一种混合方法来使参数适应细胞密度:Sadeghi 等人。使用恒定体积,但只有在达到一定的细胞密度后才开始灌注培养基。更重要的是,他们表明,当该过程以较小的体积开始时,细胞扩增的结果会更好。因此,可以通过将增加的体积与基于细胞密度或营养水平(谷氨酰胺和葡萄糖)的流量灌注相结合来开发另一种方法。有趣的是,除了可用体积外,所有参数都可以在细胞增殖时随时间调整,例如摇摆率、摇摆角、灌注流速等。
总体而言,Wave 生物反应器获得的增殖率与静态袋法相似或显着高于静态袋法,并且需要的体积更小。
除了扩增后的细胞数量外,还根据表型分析了Wave生物反应器中的 T 细胞群,重点是CD4+和CD8+ 细胞之间的平衡。
无论如何,使用该系统存在一些限制。与静态小规模工艺相比,需要许多优化步骤,涉及基本培养参数以及 Wave 生物反应器特有的不同技术参数。这种优化可能很困难,因为它们会产生各种影响:例如,摇摆率会改变剪切应力,但也会影响曝气,从而影响氧气交换。与其他系统相比,初始购买可能是一笔更大的投资,但这可能会有所不同,因为由于培养基体积减少,常规培养会更便宜。由于该系统是多个运动和灌注的组合,电气和机械故障改变细胞行为的风险更为重要,因此设置需要很强的冗余。
4.4.单系统多步骤生物反应器:Miltenyi Biotec Clinimacs Prodigy

鉴于生物反应器是在生物过程中转化物质的系统的总称,一个完整的生物反应器系统可能能够在先进的治疗生产线中执行多个步骤。
一种这样的设备 Miltenyi Biotec Clinimacs Prodigy系统。该系统能够在一件硬件及其相关的一次性管组内执行细胞选择、激活、转导、扩增、细胞收获和配制。
在Mock等人的研究中,Prodigy中获得的结果与GMP设施中使用的过程相当:Prodigy的细胞数量、活力和无菌性结果既没有改善,更重要的是,与比较中获得的结果相比有所下降。过程(包括培养袋和Wave 生物反应器)。这表明系统的好处在于一个系统中多个步骤的自动化。该系统的某些部分不仅在执行操作时通过预编程实现自动化,而且在某种程度上还受到控制:压力和液体传感器可以检测新任务何时完成;摄像头可以在离心步骤中监测细胞分离的进程;显微镜可用于评估细胞培养的进展。封闭在一个设备中的多个步骤可能会减少洁净室空间并允许在卫星位置进行生产,这有助于实现分散制造过程的好处。
Mock 等人绘制的表格。表明 Prodigy 执行的许多步骤仍然需要操作员交互,因此,它不是一个完全自动化的系统。此外,在单一系统硬件中提供多种功能可能存在缺陷。无论培养系统如何,细胞扩增都是基于T细胞的免疫疗法生产的最长阶段,假设可以有效地提供慢病毒载体 。较长的细胞扩增步骤意味着当Prodigy在细胞扩增阶段运行时,离心和细胞分离功能保持闲置。这并不理想,考虑到这些疗法目前是自体的,因此,该设备可用于为单独的患者处理材料。允许在先进疗法制造的各个步骤出现瓶颈,单系统多步骤生物反应器可能会因硬件可用性不足而限制生物加工链的吞吐量。这将鼓励未来的多步生物反应器基于所有处理链的吞吐量分析,从而最大限度地减少瓶颈的影响。
该系统的另一个显着缺点是其容量有限,这可能会限制其在生产多剂量治疗中的使用以及在生产同种异体治疗中的使用。培养容器与用于离心的单元相同,这表明这种多次使用可能不是细胞培养的最佳设计。
4.5.搅拌系统和自制设计
另一类生物反应器和动力学容器是旋转烧瓶和进一步搅拌系统(图 7)。通过机械或磁力搅拌,它们的主要优点是提供简单的几何形状,以提供均匀的培养条件和出色的气体交换,并且易于采样。市场上有不同的型号,并且可以通过增加储罐的体积轻松进行放大。灌注可以增加搅拌罐内实现的细胞密度,减少扩大细胞产量所需的体积。然而,克罗普等人研究的灌注。需要额外的硬件来保留生物反应器内的纯细胞干细胞聚集体。搅拌罐还允许在培养过程中使用 REP并且主要用于恒定的培养体积。
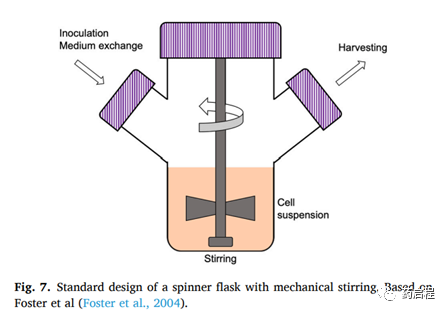
为了优化此类系统中培养的受控环境,需要调整的主要参数之一是搅拌机制的速率。高搅拌速率产生的剪切应力确实会危及培养基混合对细胞增殖的有益影响。例如,Foster等人已经研究了转速对 T 细胞培养的影响以及与基于喷射的曝气相结合。旋转烧瓶中高达120 RPM的速度范围或大规模 (2 L) 搅拌生物反应器中高达180 RPM 的速度范围在不改变细胞活力和增殖的情况下得到了成功。
除了速度外,如果在静态条件下优化后需要,还可以在搅拌系统中监测或控制许多其他参数,例如渗透压、IL-2 浓度、pH、氧张力和进料计划。可以通过修改整体培养方案以及搅拌机制来减少剪切应力的影响。Bohnenkamp等人研究了搅拌生物反应器中的不同进料策略后。表明每天更新一小部分培养基(不超过总体积的一半)比每2/3天进行一次更大的变化会导致更高的增殖率,最糟糕的方法是完全更新去除废物和旁分泌因素。因此,搅拌生物反应器的一个缺点可能是需要频繁干预介质更换,限制了封闭系统的潜力。我们可以建议将搅拌容器与培养基灌注相结合,但据我们所知,这种方法并未广泛研究用于 T 细胞扩增,尽管最近已经报道了例如干细胞。
事实上,搅拌罐生物反应器在其他细胞谱系的扩增方面已经显示出非常好的结果,特别是诱导多能干细胞 (iPSC),免疫细胞可以在体外衍生。这些方法不仅可以为免疫疗法的替代体外扩增铺平道路,而且基于 T 细胞的过程也可以从其他细胞类型的进展中受益。
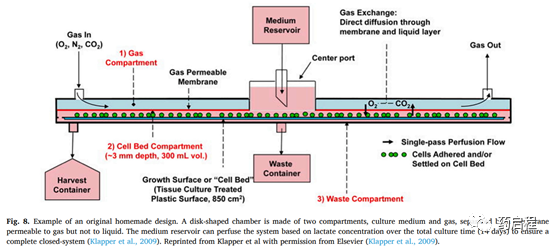
迄今为止,T细胞培养生物反应器尚未达成任何共识,并且针对封闭和自动化系统存在许多不同的改进方法。培养基和气室由可渗透气体但不可渗透液体的膜隔开(图 8),在培养过程中对两相进行灌注。培养基由 7 升存储库提供,用于14天的增殖步骤,从而形成一个完全封闭的系统。流速随着时间的推移和批次间的变化进行调整,以将乳酸浓度保持在0.5和1mg/mL 之间,缓慢和层流,对细胞悬浮液无害。该过程允许使用REP,特别是在第0天以单次推注形式注射IL-(确认封闭系统潜力)和低血清浓度,与进一步的临床验证相关。
新颖的设计可以提高生物反应器的扩展能力,尽管它们仍然存在限制它们在治疗制造中采用的局限性。
05
讨论和展望
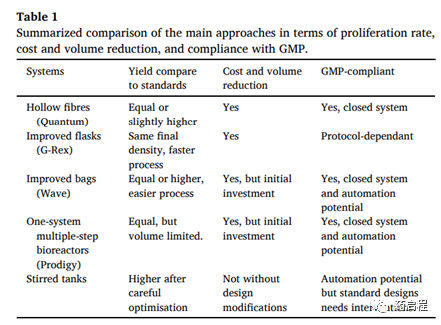
总之,作为总体结果,与静态标准相比,大多数研究的系统在 T 细胞增殖方面表现出更好的结果;或者,在类似结果的情况下,提高了易用性并降低了成本和劳动时间(表 1)。
本综述中提出的质量源于设计(QbD)和实验设计(DoE)方法将成为执行这些多参数研究的有益工具,以真正了解自体细胞疗法生产中的设计空间和操作条件。这些未来的研究还需要确定细胞扩增生物反应器及其新功能如何影响QbD原则。此外,由于REP条件广泛用于生物反应器方法,将结果与不使用REP的对照组(即没有触发 T 细胞活化和增殖的因素的基础培养基)进行比较可能会很有趣,以便研究REP和特定生物反应器特征之间可能的协同作用。这甚至可以突出先进的系统,其中可以减少激活步骤以获得相同的扩展范围,从而降低成本和劳动力。
通过使用生物反应器,可以更好地控制上述细胞培养过程中的参数。然而,由于复杂的T细胞生物学,T细胞扩增中使用的参数对所得细胞群的影响并不总是很清楚。因此,我们建议从生物反应器的初始设计和部署到生物过程中采用实验设计(DoE)方法。这种方法将允许识别影响生物反应器执行过程的所有参数,并了解如何通过有效使用实验运行来改变参数以影响输出。此外,很明显,生物反应器可以影响治疗细胞的许多质量属性。这种多属性影响需要了解设计质量 (QbD),考虑到细胞产品将有不止一个因素决定其作为治疗剂的成功,这应该从初始设计阶段开始考虑。这种方法将扩展生物反应器研究,以包括生物反应器产生的细胞的所有治疗质量方面,而不仅仅是反应器产生大量细胞的难易程度。
除了增加增殖外,对于各种生物反应器,最终目标通常是设计一个完全封闭的系统以符合GMP,但也向全自动系统迈进。例如,它可以作为 Wave生物反应器的可选模块来控制介质交换。由于多次干预,自动化设备减少了劳动工作和污染风险,但这也是获得具有批次间可靠性的标准结果的最佳方法。确实建议使用生物反应器的标准化条件来限制批次差异。
然而,通过预编程设定任务的自动化不允许系统响应偏差。可以通过引入分析技术和过程控制方法来生产改进的系统。技术瓶颈是开发无创和实时分析细胞培养参数的方法,例如细胞浓度、pH、乳酸浓度或耗氧量,这些方法可以嵌入湿润的 37℃大气中。测量将用于自动调整技术参数,如摇摆运动、速度、流速、介质更新或在体积增加的情况下注入。这使治疗生产生物反应器系统远离自动化,通过对任务进行预编程,目前是通过对上述系统的审查而建立的规范,并转向闭环控制,这是一个更强大的工程支柱。传感器和执行器不应显着增加成本或降低安全性,从而危及生物反应器在增殖率和GMP 合规性方面的优势。
有了检测质量属性的合适方法,就面临着实施提供反馈的方法的挑战,以便可以通过改进处理方面来抵消监控设备的成本。需要对自体治疗环境中的在线传感和控制反馈进行成本效益分析,以了解这些方法是否可以在自体治疗制造规模上产生有价值的改进。
当细胞构成治疗的一部分时,批次间的变异性是一个已知问题,从我们上面的回顾来看,很明显,当前一代生物反应器可以稳定参数并自动为每批扩增的细胞在相同的程序中执行任务无论使用的确切设计如何。然而,它们中的许多缺乏闭环控制来响应不断进行的细胞扩增,不同批次的进展速度可能会有很大差异,这在本文中引用的生物反应器研究中得到了广泛报道。缺乏控制的原因与缺乏传感器和已建立的方法来执行细胞扩增过程的在线采样有关。
为了进一步迈向临床,考虑附带步骤也很重要,例如在使用冷冻保存细胞时如何改变生物反应器的产量和活力。额外的恢复期可能必须包括在培养计划中。
06
结论
总之,虽然大多数报告的系统显示出比当前黄金标准更高的增殖率,但目前尚未就获得临床相关T细胞数量的最佳生物反应器方法达成共识。然而,最佳细胞密度和增殖率并不是确保转化进展的唯一目标:自动化、过程控制和完整的封闭系统仍未实现最终目标,但如果从开发的早期阶段考虑,可以逐步实施,因为它是 以前做符合GMP和REP,现在广泛使用。建议使用过程工程方法来帮助克服实施新一代生物反应器技术的挑战。
DOI:10.1016/j.biotechadv.2021.107735
编辑:小果果,转载请注明出处:https://www.cells88.com/cells/myxb/6851.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫