累趴的T细胞
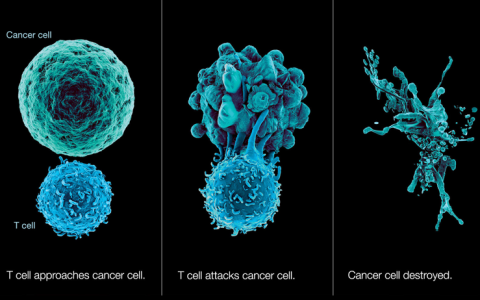
每个人的身体内部都有一支隶属于我们个人的专属军队——免疫细胞,为保卫我们的健康冲锋陷阵,万死不辞。在众多免疫细胞中,T细胞是不可或缺的一员大将。但T细胞也有累了的时候,我们如何理解“T细胞耗竭”?
我们通常所说的 T 细胞耗竭(T Cell Exhaustion)就是指,因长期慢性感染或癌症,导致患者体内T细胞功能丧失的情况。由于长期暴露于持续性抗原或慢性炎症,T细胞逐渐失去效应功能,记忆T细胞特征也开始缺失。T细胞耗竭是可以逆转的,至少可以部分逆转,主要是通过阻止PD-1之类的抑制性通路。
–01–
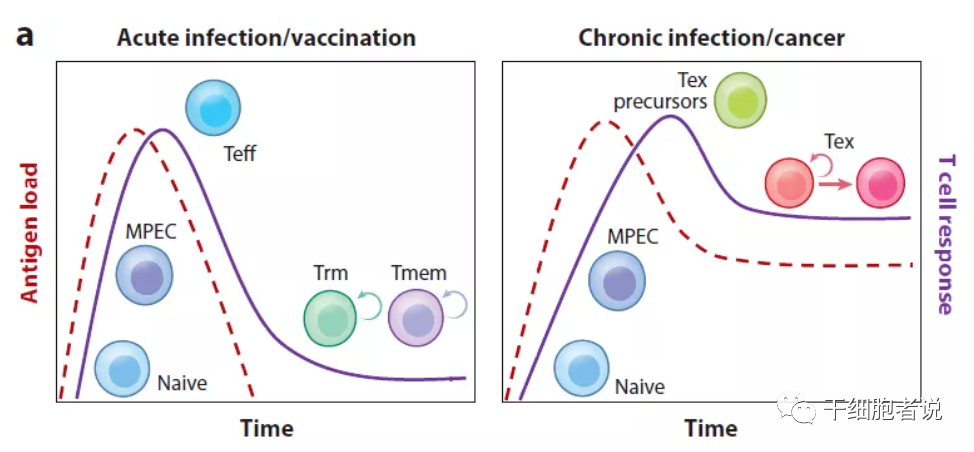
抗原的持续作用于T细胞耗竭
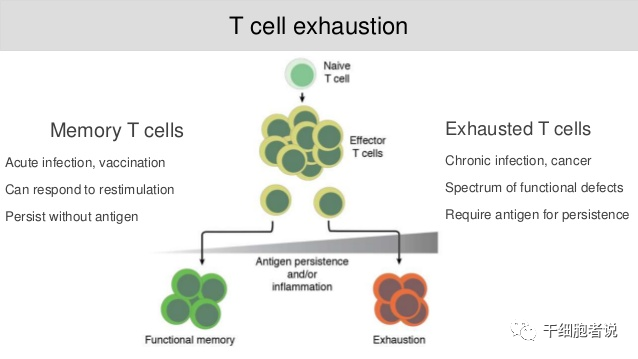
T细胞耗竭与抗原的持续驱动作用息息相关。感染后,初始T细胞经过抗原、共刺激和炎症激活,以指数方式增殖形成效应T细胞亚群。
在急性感染或接种疫苗时,当炎症消退或抗原清除后,某些效应T细胞会分化成功能性记忆T细胞,其可产生细胞因子(如IFN-γ、TNF和IL-2等),如同身经百战的老兵,继续巡逻在身体内。如果后续发生感染,很快产生强烈的免疫反应。
在慢性感染或癌症期间,由于长期暴露于持续性抗原和炎症,T细胞受到持续刺激,精疲力竭的效应T细胞逐渐失去效应功能,记忆T细胞特征也开始缺失,T细胞耗竭发生了。
耗竭T细胞(发生耗竭的T细胞)在功能上有别于效应T细胞和记忆T细胞,其特点是效应功能丧失,抑制性受体(IRS)表达增高且持续,表观遗传和转录谱改变,代谢方式改变。T细胞衰竭是癌症病人免疫功能障碍主要因素之一。
T细胞是否会发生耗竭,主要受表达的抑制性受体(IRS)的水平和数量的影响,而免疫检查点抑制剂可以部分逆转T细胞耗竭状态。此外,抗原刺激的强度和感染持续时间也是重要因素。
–02–
T细胞耗竭的机制概览
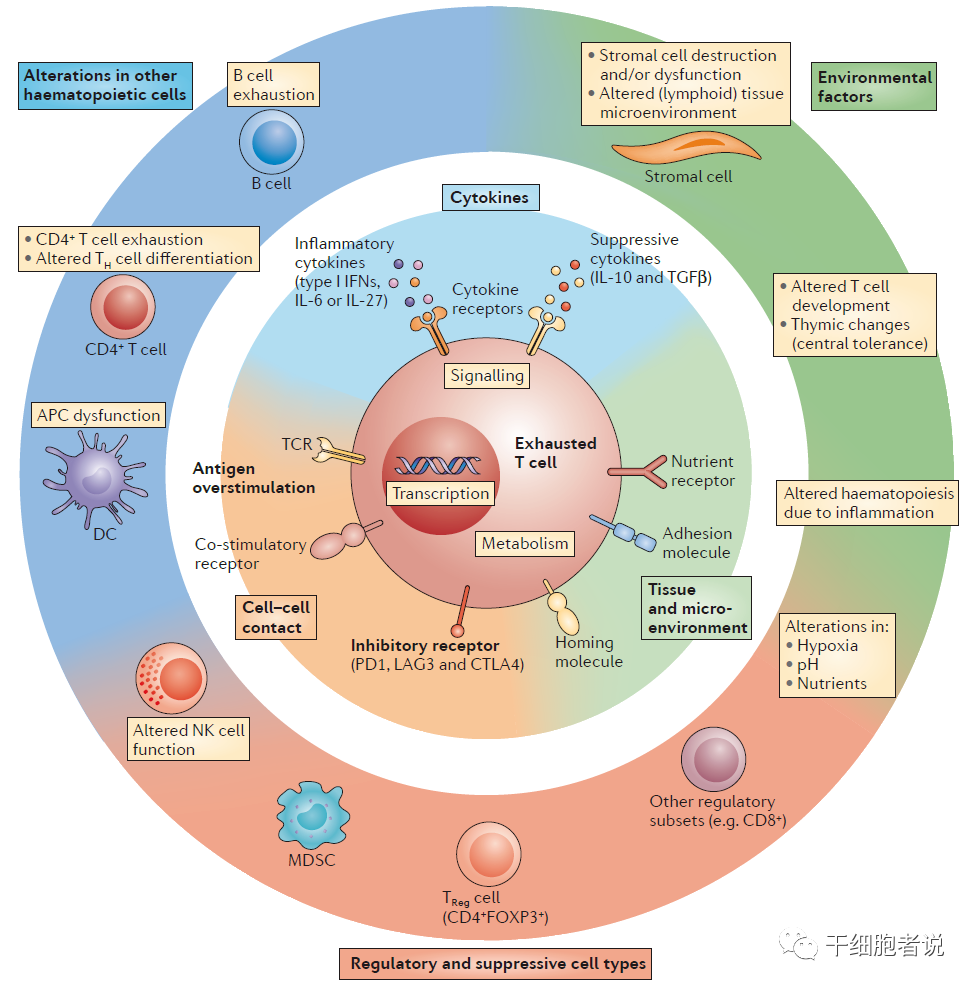
(1)细胞间的信号(T细胞受体接合时间延长、共刺激和/或共抑制信号)
微环境影响可能包括组织分布和/或迁移模式改变,并导致感应氧张力的途径(肿瘤抑制因子和/或缺氧诱导因子途径)、pH和营养水平改变。组织破坏和淋巴组织改变可能起主要作用。
引起T细胞耗竭的原因可能是其他免疫细胞和基质细胞,除了CD8+T细胞耗竭参与已被证实,其他细胞包括:CD4+T细胞、NK细胞、抗原呈递细胞(APC)、B细胞和调节细胞(例如骨髓来源的抑制细胞MDSC>和调节性T细胞Treg>)。
–03–
T细胞耗竭的调控因素
慢性感染或癌症的一个关键特征:由于长期暴露于持续性抗原和炎症,T细胞受到持续刺激。效应T细胞失去效应功能,记忆T细胞特征缺失。造成T细胞耗竭主要原因是:T细胞功能缺陷(免疫异型性受体表达增加,如PD-1、CTLA4、TIM-3),可溶性免疫抑制因子(如IL-10、IL-35增加),与其他免疫细胞的互动(如Treg细胞的抑制活性),共同造成了T细胞耗竭状态。
新的证据也表明:耗竭T细胞表现出明显的表观遗传特征,这可能导致对免疫治疗的不良反应。抑制性受体表达增加是造成T细胞耗竭的主要原因,而免疫检查点抑制剂可以部分逆转T细胞耗竭状态。
▉ PD-1/PD-LI
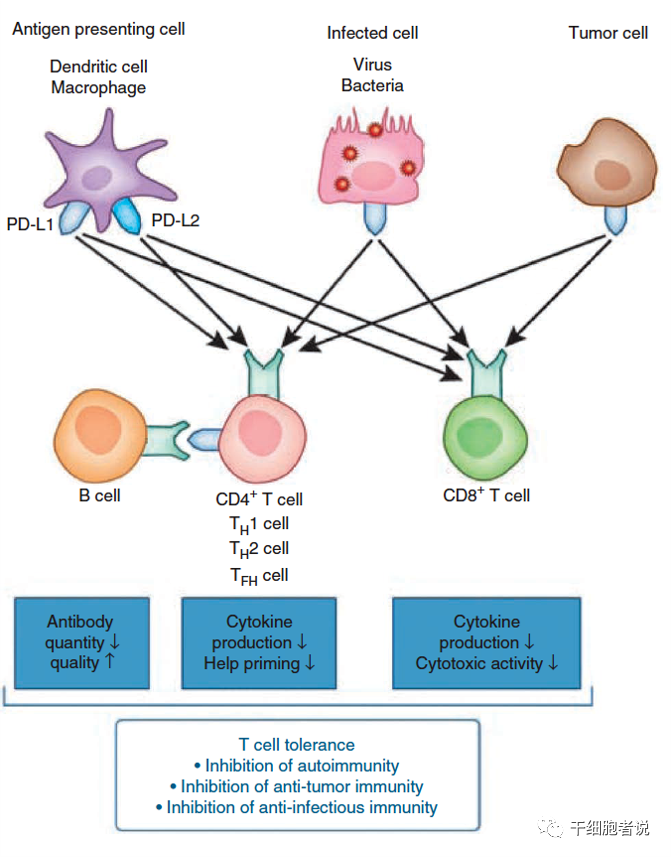
PD-1/PD-L1相互作用可诱导下游酪氨酸激酶(SYK)和磷酸酰基醇-3 激酶(PI3K)磷酸化,从而抑制下游信号传导和T细胞的生物学功能,从而促进T细胞耗竭和凋亡;促进Treg细胞增殖和免疫抑制作用,抑制NK细胞和B细胞作用。
▉ PD-1/CTLA-4
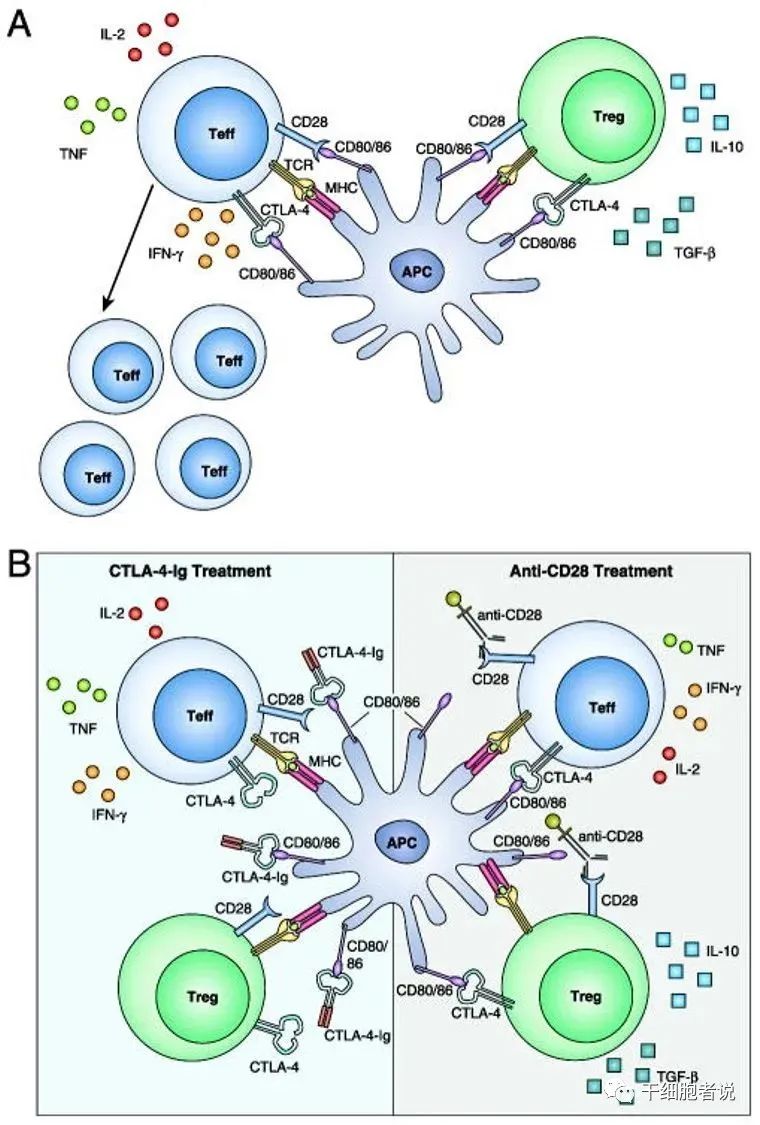
CTLA-4激活磷脂酰肌醇激酶-3(PI3-K),造成T细胞功能丧失;CTLA-4结合TCR,导致条件性T细胞扩增,并将天然CD4+CD25+T细胞转为Treg,从而抑制效应T细胞。
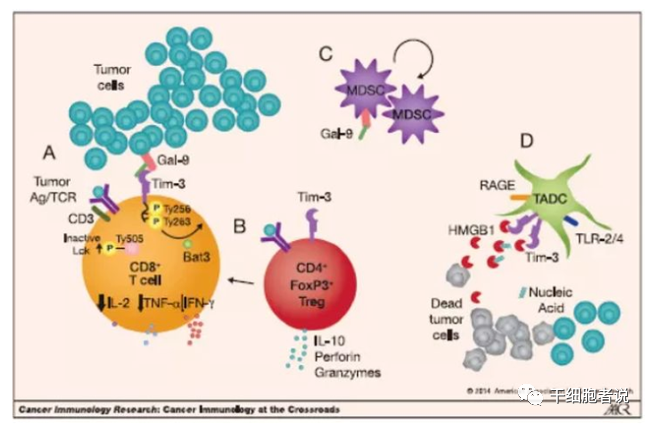
▉ IL-10
IL-10常与减弱T细胞活化有关,阻断IL-10可预防和/或逆转 T 细胞耗竭。DC细胞、B细胞、单核细胞、CD8+T细胞和非调节性CD4+T细胞都能产生IL-10。IL-10的作用可直接作用于T细胞,也可通过APC间接作用于T细胞,或两者兼有。
–04–
如何遏制T细胞耗竭
▉ 免疫检查点抑制剂可逆转T细胞耗竭状态
耗竭T细胞表达免疫抑制性受体,免疫检查点抑制剂可以阻断这些信号,逆转耗竭的T细胞,恢复肿瘤微环境肿瘤浸润T细胞(TIL)功能。
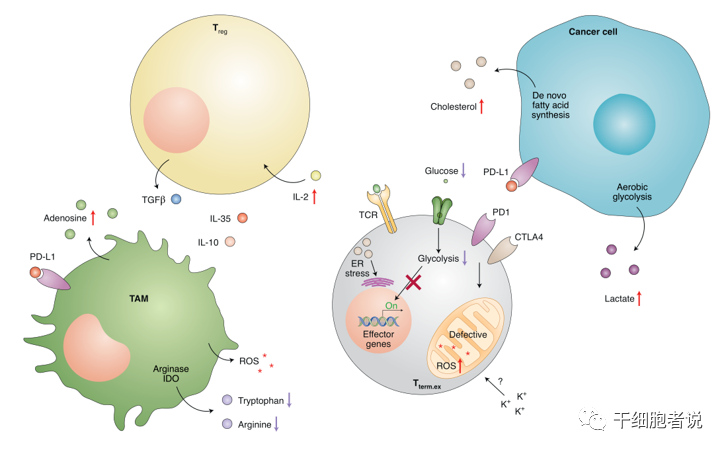
T细胞耗竭的主要原因为免疫抑制性受体表达增加,如PD-1、CTLA-4、Tim-3等,联合受体抑制剂治疗可以增强免疫治疗效果。
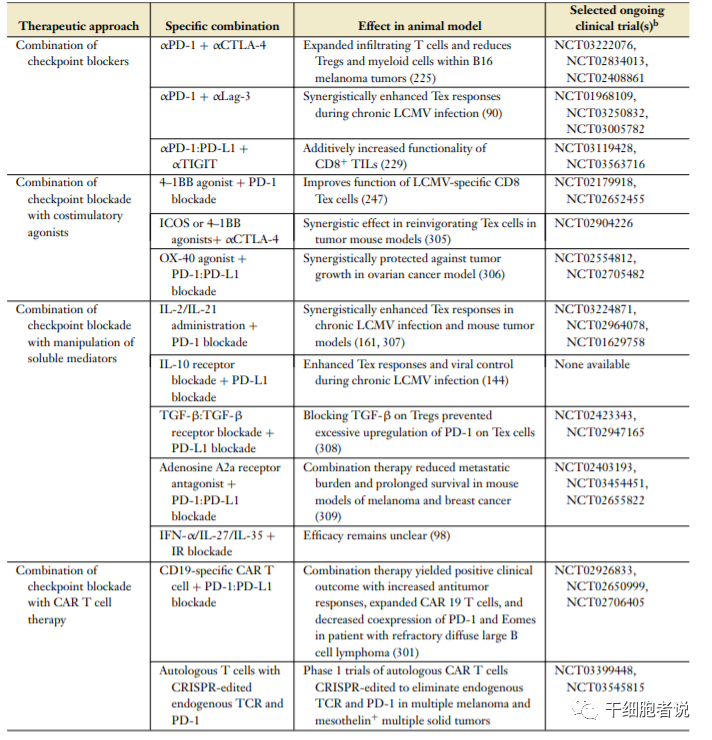 免疫联合疗法部分临床试验
免疫联合疗法部分临床试验–05–
文末的话
T细胞衰竭机制复杂,因素众多。根本原因还是抗原和炎症长期刺激 T 细胞,T细胞厌倦了这样的生活,开始躺平,不愿意搭理这些抗原或炎症,效应T细胞不再效应,记忆T细胞也不再记忆。
其实,人何尝不是如此。当你长期处于焦虑状态,体内源源不断给你提供免疫抑制剂和神经抑制剂,你的免疫系统和神经系统将持续低下。虽然我无法证实这件事,但人还是要开心一点,远离焦虑!耗竭的T细胞就是榜样。
参考文献:
-
http://www.bloodjournal.org/Thorsten Zenz -
Annu. Rev. Immunol. 2019. 37:457–95 -
Nature Reviews Clinical Oncology, 2016, 13(4):202-203. -
Nat Immunol. 2013 Dec;14(12):1212-8. -
Nat Metab 2, 1001–1012(2020). -
Annu Rev Immunol. 2019 Apr 26;37:457-495.
编辑:小果果,转载请注明出处:https://www.cells88.com/cells/myxb/13103.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫