2021年6月22日,复星凯特CAR-T细胞治疗产品益基利仑赛注射液已正式获得批准。中国迎来首款获批上市的CAR-T细胞治疗产品。
作为另一种价值的免疫细胞,NK细胞也逐渐受到关注,在国际上有众多的临床研究进展。NK细胞具有广谱的抗肿瘤作用。目前,基于NK细胞的肿瘤免疫疗法逐渐被挖掘出来。今天我们就来聊一聊究竟NK细胞疗法和CAR-NK细胞疗法。
自然杀伤细胞(Natural killer cell,NK细胞 ),是除 T细胞、B细胞之外的第三大类淋巴细胞,不仅与抗肿瘤、抗病毒感染和免疫调节有关,甚至参与超敏反应和自身免疫性疾病的发生。
–01–
NK细胞的发育和分类
NK细胞在机体内由CD34+造血祖细胞(HPC)发育而来,是一个连续的过程,共同淋巴细胞祖细胞(CLPs)逐渐下调CD34,上调CD56,促使NK细胞分化与成熟。
在小鼠中,共同淋巴样祖细胞产生共同ILC前体(Common ILC precursor, CILCP)。而CILCP可产生NK细胞、辅助样ILCs。从CILCP开始,机体内的NK细胞发育至少包括五个阶段才可产生NK细胞,即:NKP→rNKP→CD27+CD11b−NK→CD27+CD11b+NK→CD27−CD11b+NK
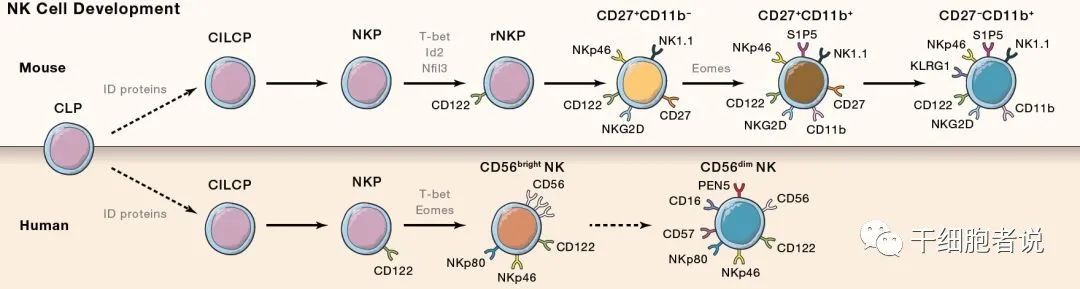
在人类中,一个接近CLPs的多能祖细胞能够产生ILCs的所有亚群。从CLPs发展出 ILC 限制的CILCP,进而产生NK限制的NKP。NKs的特征是CD122的表达以及CD34和CD127的丢失。T-bet和Eomes的表达是进一步分化为功能性NK细胞所必需的。
CD56的表达可以分两个NK细胞亚群,CD56dim和CD56bright,其中CD56- NK细胞具有抗肿瘤细胞毒性,并且两个亚群都能够产生细胞因子。两种活化表面受体NKp46和NKp80在两种NK细胞亚群中均有表达。CD56bright NK细胞通过获得CD16、PEN5和CD57的表达而分化为CD56dim NK细胞。
–02–
NK细胞的生物学功能
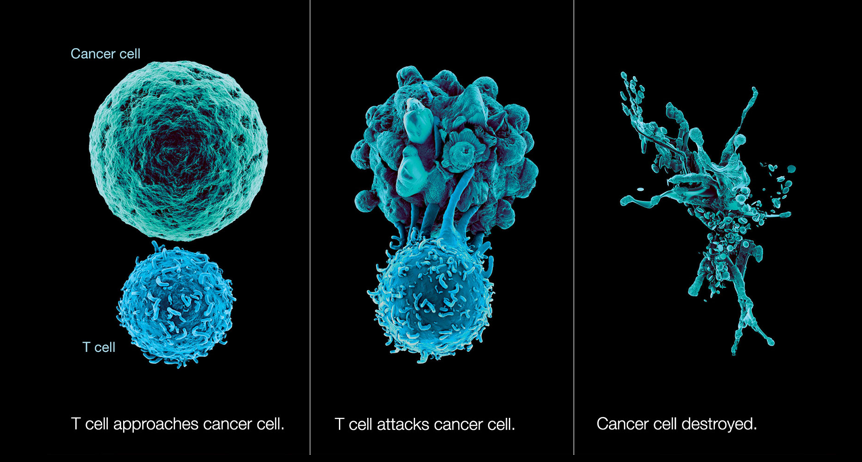
NK细胞大多数具有抗肿瘤细胞毒性。它们可产生大量分子(如穿孔素、颗粒酶、人体颗粒溶素等)的溶解颗粒,这些分子可诱导应激细胞的细胞死亡。NK细胞也表达多种肿瘤坏死因子(TNF),如FASL和TRAIL,分别与相应的受体FAS或TRAILR结合诱导靶细胞凋亡。此外,NK细胞产生一系列细胞因子(如IFN-γ、TNFα、IL-10)、生长因子(如GM-CSF)和趋化因子(如CCL3、CCL4、CCL5、XCL1)。
NK细胞可以通过与DC细胞、巨噬细胞和T细胞相互作用来形成免疫反应。细胞表面抑制性和激活受体之间的动态平衡保证了NK细胞效应功能的调节。这些抑制性受体,可识别各种形式的MHC-I分子。因此,靶细胞上MHC-I分子的减少或缺失可降低源于NK细胞的抑制性信号的强度,因此促进NK细胞的激活。激活性受体和天然细胞毒性受体的参与也会导致NK细胞的激活。
NK细胞还可介导抗体依赖细胞介导的细胞毒作用(ADCC),同时也是目前热门抗体药物发挥临床效果的重要作用机制。
–03–
基于NK细胞的治疗策略
作为抗癌的第一道防线,NK细胞已经成为免疫治疗临床试验中重要的一环,2000年,科学家研究证实小鼠癌症的发生和NK细胞自身的缺陷有关。
随着NK细胞抗肿瘤方面的探索愈发深入,越来越多的临床研究者希望了解NK细胞是如何对抗肿瘤的。当然,由于NK细胞抗癌的普遍性,所以近年来NK细胞用于治疗癌症的种类也愈发多样化。这也使得NK细胞疗法很可能会像PD-1/PD-L1抑制剂一样,在未来成为广谱抗癌药的一种。
依据NK细胞的抗肿瘤特性,目前已经开发了几种治疗策略。
-
细胞因子:IL-2和IL-15,可提高机体内NK细胞活性,但潜在的恶化免疫反应是一个安全问题。 -
活化的NK细胞:将健康捐赠者的NK细胞在体外以IL-2和IL-15刺激后,再输住到癌症患者的血液中。 -
基因工程化NK细胞:CAR-NK细胞转基因表达抗B细胞恶性肿瘤的抗CD19或抗CD20受体,IL-2和IL-15增强NK细胞存活,或NKG2D提高肿瘤识别和溶解等不同治疗策略均正在临床试验进行中。 -
单克隆抗体:针对肿瘤相关抗原的治疗性抗体,如分别识别CD20和EGF受体的利妥昔单抗或西妥昔单抗,可通过NK细胞诱导ADCC。针对抑制分子的抗体,如识别NKG2A的单抗,可增强NK细胞的反应。调控NK细胞检查点的大分子药物亦正在开发中。 -
NK细胞衔接器:靶向肿瘤抗原(如CD19、CD20或EGFR)、NKp46和CD16的多功能抗体将肿瘤细胞和NK细胞结合在一起,从而触发毒杀肿瘤细胞机制和促进NK细胞分泌细胞因子。
–04–
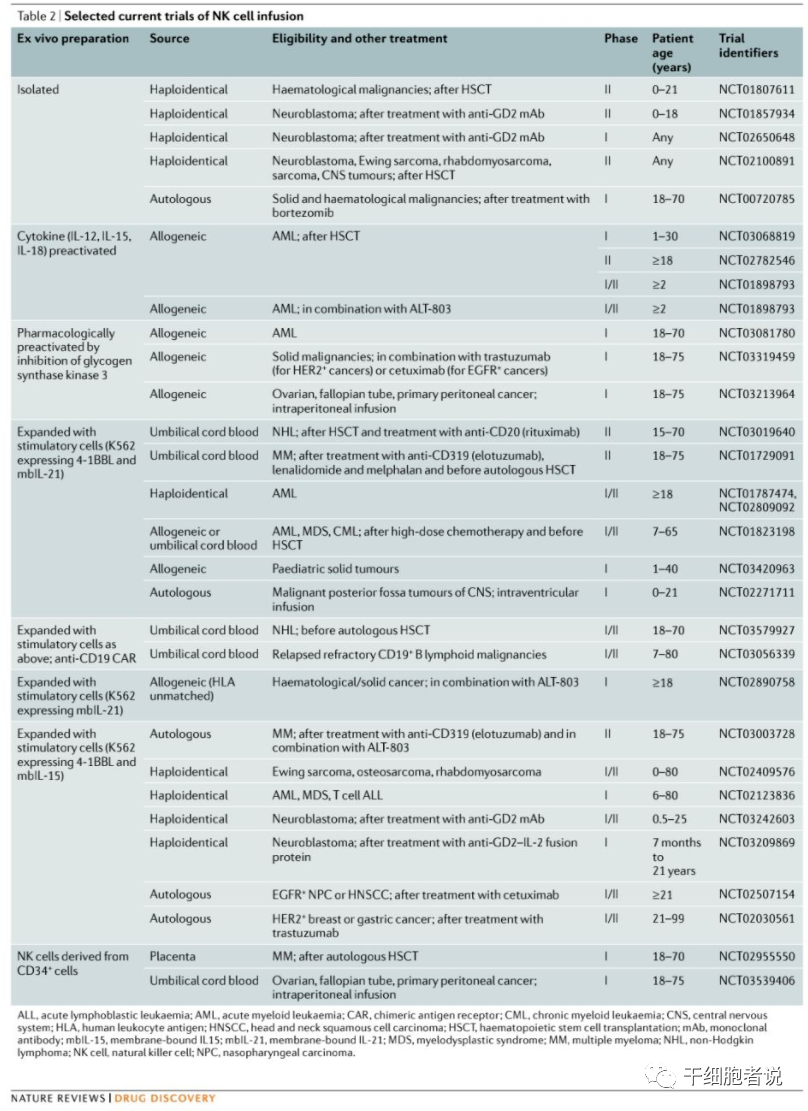
–05–
CAR-NK细胞疗法
NK细胞成为了研究人员开发新型免疫疗法的理想选择之一。目前,正在开发的NK细胞治疗产品主要有两类:一类是自体或是异体NK细胞治疗产品,另一类是CAR-NK产品。
就像CAR-T细胞疗法,CAR-NK细胞同样是给NK细胞加装了对应的癌细胞靶向的嵌合抗原受体(CAR),帮助NK细胞更精准的找到肿瘤细胞。CAR-NK细胞是在CAR-T细胞疗法相对成熟之后,逐渐发展起来的。在临床前和临床试验中,CAR-NK细胞疗法当之无愧成为细胞疗法中的热门选手。
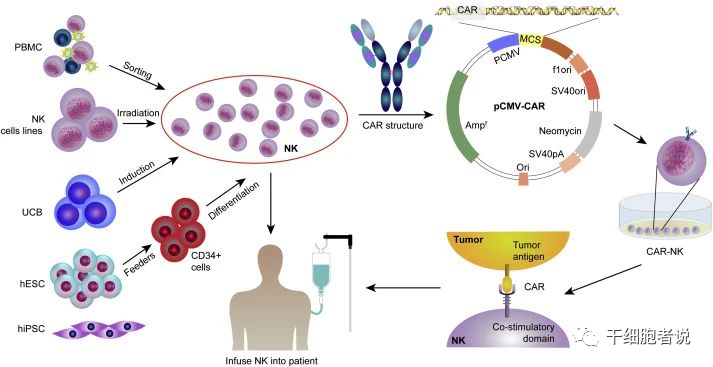
CAR-NK细胞的来源和产生过程
CAR-NK细胞治疗产品具有以下几个潜在优势:
-
第一,CAR-NK细胞免疫治疗具有更好的安全性。
-
第二,CAR-NK细胞仍具有天然的抗肿瘤细胞的毒性,除了以CAR-依赖的方式杀死肿瘤靶细胞外,CAR-NK细胞还可以通过非CAR-依赖的方式消灭癌细胞。
-
第三,具有成为“通用型”产品的潜力。
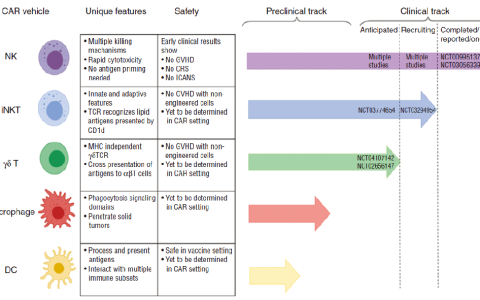
根据ClinicalTrials.gov网站公示信息,目前已有许多CAR-NK产品的临床试验正在开展中,大部分处于1/2期临床试验阶段。靶点多数是常见的恶性血液癌症靶点,如CD19、CD22、BCMA、CD33等。还有一些CAR-NK产品靶向的是实体肿瘤相关抗原,如PSMA、间皮素、ROBO1、NKG2D等。CAR-NK细胞在肿瘤中的作用正在被广泛研究(如下图)。
血液瘤中的临床前研究
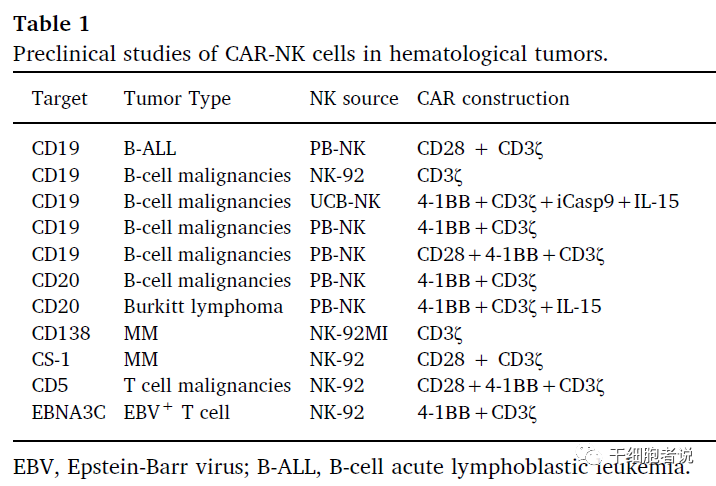
CAR-NK细胞在血液瘤中的临床前研究
实体瘤中的临床前研究
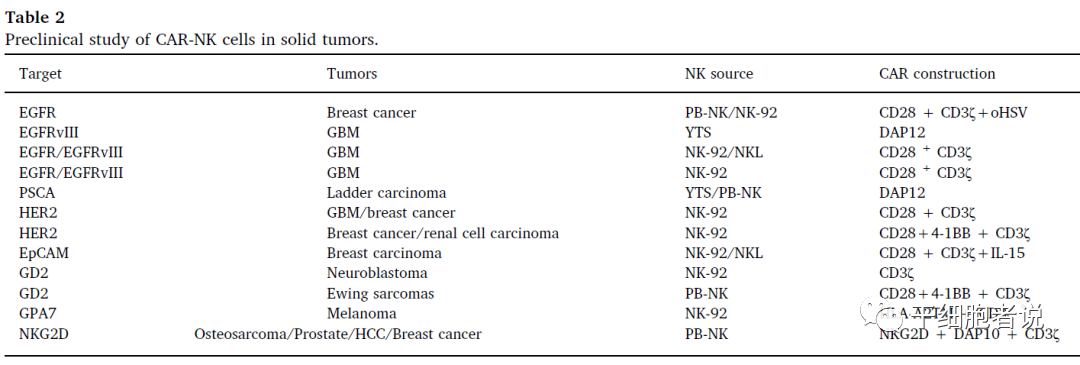
CAR-NK细胞在实体中的瘤临床前研究
CAR-NK的临床研究
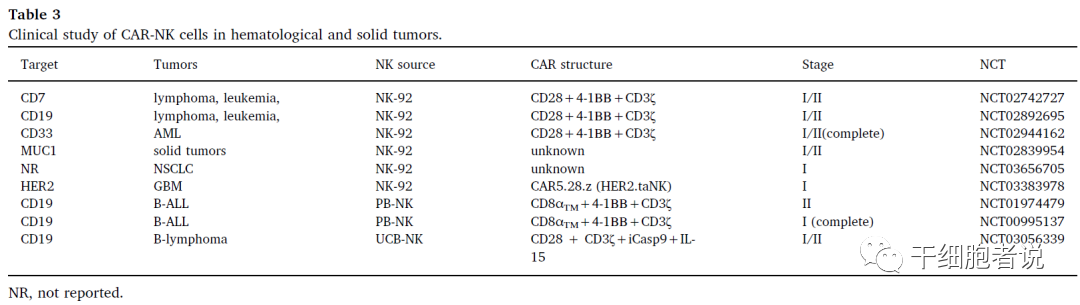
CAR-NK细胞在血液瘤和实体瘤中的临床研究
–06–
文末
NK 细胞具有独特的抗肿瘤效应,不受MHC限制的细胞毒性、产生细胞因子和免疫记忆等功能,使其成为先天性和适应性免疫反应系统中的关键角色。
CAR-NK 细胞疗法是一个很有前途的临床研究领域,对某些癌症患者具有良好的安全性和初步疗效。相信,CAR-NK细胞疗法可能会导致肿瘤免疫治疗的革命性进展。
参考资料:
[1] Niklas K. Björkström et al. Emerging insights into natural killer cells in human peripheral tissues. Nature Reviews Immunology (2016).
[2] SnapShot: Natural Killer Cells(来源:Cell)
[3] 医药魔方pro公众号
[4]CAR-NK for tumor immunotherapy: Clinicaltransformation and future prospects[J].Cancer Letters Volume 472, 1 March 2020, Pages 175-180.
[5]CAR-expressing NK cells for cancer therapy: a new hope. BiosciTrends. 2020 Sep 6.
[6]. Natural Born Killers: NK Cells in Cancer Therapy. Cancers (Basel). 2020 Jul 31;12(8):2131
编辑:小果果,转载请注明出处:https://www.cells88.com/cells/myxb/11268.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫