脑卒中严重危害人类健康和生命,是我国成年人致死和致残的首位原因,且发病率逐年增高。缺血性脑卒中发作后,随着时间的推移大多数患者会出现一定程度的自我恢复。
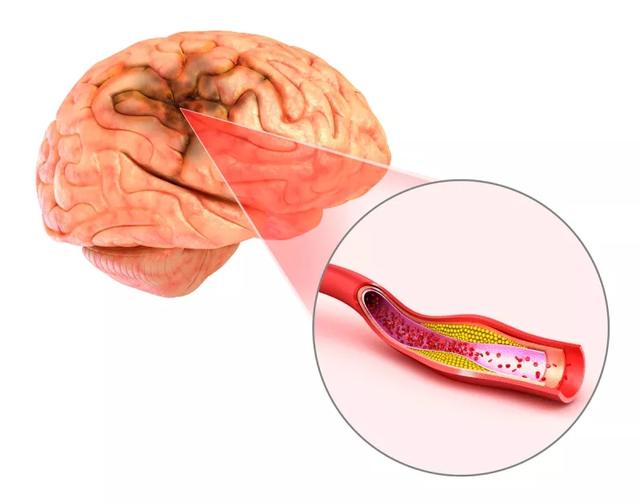
缺血性脑卒中主要由大脑供血中断及脑缺血引 起,其发病率高且预后效果不好。缺血脑组织的神经修复主要包括血管生成和神经发生,促进损伤区域的神经功能恢复。
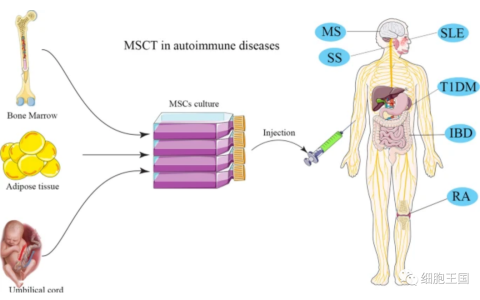
针对脑缺血后神经修复的研究内容日趋丰富,干细胞疗法成为改善缺血性脑卒中预后的新途径,其中间充质干细胞(MSCs)尤其是骨髓来源的间充质干细胞 (BMSCs)的应用最为 广泛,可以在多个方面减轻脑组织损伤并促进神经修复。

MSCs促进脑缺血后神经修复三大机制
MSCs促进脑缺血后血管生成
微血管生成可增加损伤区域大脑血流量和营养物质供应。在血管生成过程中,最初的血管丛通过 发芽、分支、修剪、内皮细胞生长以及细胞募集形成成熟的血管,而脑缺血后血管生成则是从原有血管上分支而来。血管生成和血管成熟受到VEGF及其 受体以及血管生成素l(An91)/Tie2 系统的调控。
研究表明,利用大脑中动脉闭塞 (MCAO)模型导致大鼠脑缺血后,立即脑内注射BMSCs,7d后脑内VEGF的表达显著升高并促进了血管重塑旧。大鼠脑缺血 后24 h内注射人源BMSCs,脑缺血区域VEGF,Angl和Tie2的表达增多,增强新生血管的稳定性,增强的血管新生从而改善了卒中后神经修复【1】。
BMSCs促进脑缺血后神经修复
脑缺血后神经元的可塑性代表大脑的修复能力,其强弱与脑内其他细胞(如星形胶质细胞和小胶质细等胞)的变化也有关。BMscs可以通过 释放营养和生长因子,例如VEGF,BDNF和bFGF等增强脑缺血后大脑可塑性,同时还可以通过抑制促炎因子的表达等促进神经修复。这些因子不仅促进了血管的生成,也影响神经修复过程,包括提高神经元的可塑性、促进神经胶质细胞功能恢复、减轻脑部炎症等,在NVU整体上发挥作用。
BMSCs促进神经祖细胞迁移与神经新生研究发现,将BMSCs移植到MCAO模型大鼠同侧脑组织中,可增加缺血脑 组织中BDNF、重组人神经营养蛋白-3和VEGF等因子的表达,促进NSC增殖。在许多组织中,基 质细胞衍生因子一1α(stromal cell-derived facto-1α, SDF-1α)及其细胞受体趋化因子受体4(chemokine receptor4,CxCR4)已被证明可以指导与损伤修复相关的干细胞的迁移。BMscs减轻神经炎症研究发现,BMSCs可以通过抑制内皮细胞表达细胞黏附因子-l,减轻中性粒细胞浸润,下调MMP-9的表达从而抑制炎症反应并减轻BBB的损伤。BMSCs通过外泌体促进神经修复
在对缺血性脑卒中的研究中发现,静脉输入干细胞囊泡具有神经保护作用,说明干细胞诱导的神 经系统恢复不仅是细胞再生的结果,还可以通过旁分泌发挥作用。
有研究证明,miR一17—92转染后的BM—scs分泌的外泌体与未转染的BMscs分泌的外泌体相比,前者促进神经功能恢复能力更强【2】。这些研究表明,外泌体及外泌体内所包含的micmRNA可能是BMSCs促进神经修复的关键。

展望
BMSCs在治疗缺血性脑卒中和促进神经功能恢复方面有显著作用,并且能在脑缺血发生以后应用,在治疗疾病方面BMscs也拥有许多优势,它不仅具有强大的增殖和分化潜能,且来源非常丰富,其 自身的低免疫原性的特点也减少了很多应用风险。此外,BMScs体外培养方法相对简单,易于改造,对BMscs进行修饰可以提高BMscs的作用效果,为 BMSCs的应用提供了新的思路。
参考
【1】:MOISAN A。FAVRE I,ROME C.以nZ.Intravenous iniection of clinical grade human MSCs after experjmental stmko:functional benefit and microvascular effect[J]. cezf‰唧f口n£,2016,25 (12):2157—2171.【2】:XIN H,KATAKOWSKI M.WANG F.封口f.MicroRNA cluster miR.17.92 cluster jn exosomes enhance neuroplasticity 8nd fhnc. 1jonal recovery after stroke in mts[J].s£rok,2017,48(3): 747—753.
编辑:小果果,转载请注明出处:https://www.cells88.com/cells/gxb/3222.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫